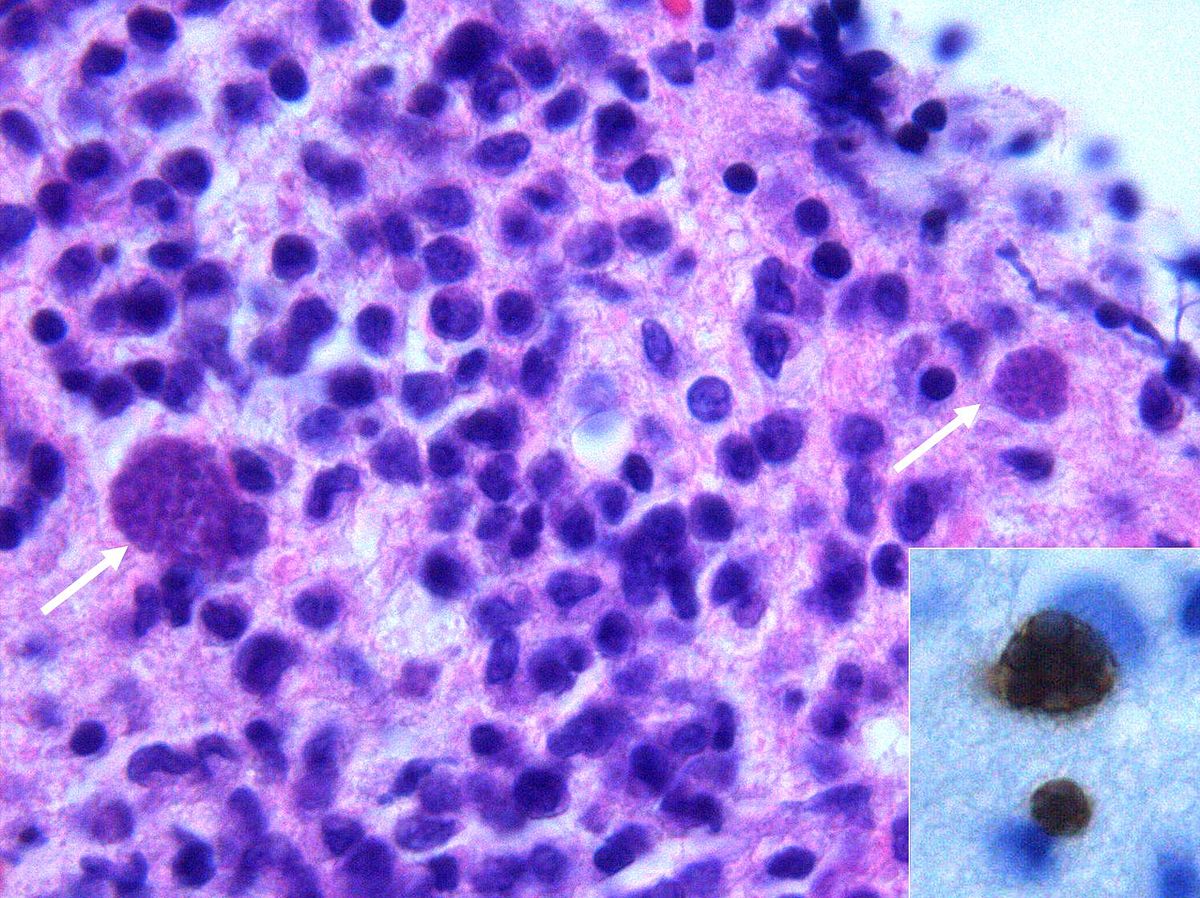
Toxoplasmose - Définition
La liste des auteurs de cet article est disponible ici.
Formes de la maladie
Il existe trois formes cliniques de la maladie qui sont :
- la toxoplasmose acquise, chez une personne ayant des défenses immunitaires normales, en général inapparente ou sans gravité
- la toxoplasmose congénitale qui peut être à l’origine de fœtopathies graves, due à l'infection du fœtus d'une femme enceinte séronégative, non protégée car n'ayant jamais été en contact avec le toxoplasme
- la toxoplasmose de l’immunodéprimé, telles que les personnes atteintes du SIDA ou les personnes greffées et traitées par des médicaments immunodépresseurs.
Toxoplasmose acquise de l’immunocompétent
Lorsque la toxoplasmose se déclenche pour la première fois chez un individu, elle est inapparente (asymptomatique) dans près de 80 % des cas : il n’y a pas de poussée de fièvre ; des ganglions cervicaux sont perceptibles pendant une semaine environ.
Dans un peu moins de 20 % des cas, la maladie prend une forme dite subaiguë ; après une incubation silencieuse de quelques jours apparaissent des adénopathies cervicales, une fièvre prolongée à 38 °C, une fatigue intense (asthénie). Le taux des monocytes augmente et la maladie est très comparable, dans ses manifestations cliniques, à une mononucléose infectieuse. La guérison est relativement lente.
Enfin, dans de rares cas, surtout chez les patients immunodéprimés et les personnes au stade sida, la maladie prend une forme dite aiguë, avec de la fièvre. Elle peut alors provoquer divers types de lésions : oculaires (choriorétinite), cardiaques, pulmonaires, voire entraîner des symptômes neurologiques. La durée de la phase de septicémie est plus longue ; les fluides corporels (l'urine, les larmes, le lait, la salive) contiennent assez de parasites pour qu'un comptage direct puisse être effectué. Selon un article de Science du 15 décembre 2006, ces cas sont dus (chez la souris de laboratoire) à une mutation d'une ou deux protéines kinases produite par le gène ROP18, lesquelles sous cette forme « anormale » perturbent la communication dans la cellule et favorise la duplication du parasite, même chez des individus en bonne santé.
Dans tous les cas, les kystes formés persistent et sont indétectables ; l'immunité du sujet à de nouvelles attaques de la maladie est conférée par la présence d'immunoglobuline G (IgG).
Toxoplasmose et grossesse
On estime, en France, qu'un enfant sur mille naît infecté par le toxoplasme.
Le risque de contamination du fœtus survient probablement lorsque la femme enceinte est en phase parasitémique, mais aussi au début de l'infection alors que la mère est asymptomatique : les parasites peuvent alors coloniser le placenta, puis, de là, parvenir au fœtus. Ce type de contamination ne survient que lorsque la mère contracte la maladie en cours de grossesse (on parle alors de toxoplasmose gravidique), bien que très exceptionnellement, la réactivation de kystes puisse conduire à une transmission du parasite vers l'enfant.
Le risque de passage de la barrière placentaire augmente au cours de la grossesse (il est faible au cours du premier trimestre (6 % à 13 semaines d'aménorrhée, et croît les mois suivants jusqu'à atteindre 72 % à 36 semaines d'aménorrhée), mais en parallèle, les conséquences sont d'autant plus graves que le fœtus est jeune, tant qu'il ne dispose pas d'un système immunitaire complet. La contamination vers la fin de la grossesse peut conduire à des formes bénignes ou à des formes latentes. Un tiers des mères qui ont fait une séroconversion en cours de grossesse donnent naissance à un enfant infecté.
Il est bon de rappeler que la toxoplasmose congénitale grave est rare et que celle-ci est souvent diagnostiquée en anténatal. Enfin, de nombreuses études sont en cours pour s'assurer de l'efficacité des traitements proposés (soit interruption médicale de grossesse en cas de forme sévère in utero, soit traitement médicamenteux en cours de grossesse).
La France est (en 2008) un des rares pays au monde à recommander le dépistage systématique des femmes non-immunisées contre la toxoplasmose, avant et au début de la grossesse ; la surveillance est ensuite mensuelle chez les femmes séronégatives pour diagnostiquer rapidement une séroconversion. Cette attitude permet de déterminer la prévalence de l'immunité contre l'infection ; elle est directement en rapport avec les habitudes alimentaires et n'a pas de relation avec les chats. Cette séroprévalence diminue avec le temps (82 % en 1960, 66 % en 1982, 54 % en 1995 et 44 % en 2003), et les séroconversions en cours de grossesse diminuent (40 pour 1 000 femmes séronégatives en 1960, 13,2 pour mille en 1995.
Contamination au premier trimestre : avant 16 semaines
C'est surtout au premier trimestre et avant 10 semaines d'aménorrhée que les risques sont importants. Dans ce cas le risque est faible mais sévère.
Les conséquences d'une telle contamination, dont le risque est faible, sont particulièrement graves : elles peuvent notamment entraîner la mort in utero ou dans les mois qui suivent la naissance, ou bien provoquer des retards psychomoteurs graves, liés à l'action du parasite sur la formation du système nerveux central (modifications de l'aspect et du volume du crâne, par des calcifications intracrâniennes caractéristiques de la toxoplasmose congénitale, hydrocéphalie, microcéphalie, dilatation ventriculaire). Au niveau neurologique, on peut constater des convulsions, de l'hypertonie ou de l'hypotonie, une modification des réflexes, des troubles végétatifs ou encore des troubles oculaires (dans 80 % des cas, une choriorétinite pigmentaire).
Contamination au second trimestre : entre 16 et 28 semaines
Une atteinte cérébrale est toujours possible mais plus rare. On ne retrouve pas au cours de la surveillance échographique des dilatations ventriculaires lorsque la séroconversion survient après 24 semaines cependant des calcifications intracrâniennes et une choriorétinite.
Contamination au dernier trimestre : après 28 semaines
Le risque est essentiellement ophtalmologique : choriorétinite pigmentaire (atteinte des pigments de la rétine). Ce risque persiste pendant plusieurs années imposant une surveillance longue de ces enfants. Les lésions oculaires sont généralement faciles à reconnaître mais il existe des formes cliniques qui peuvent égarer le diagnostic. Classiquement, on découvre une lésion jaunâtre qui peut être paramaculaire ou parapapillaire et cette anomalie va évoluer vers une cicatrisation pigmentée.
Diagnostic de la toxoplasmose congénitale
Il repose sur une démarche en deux temps.
Faire le diagnostic d'infection toxoplasmique acquise au cours de la grossesse
En l'absence habituelle de signe clinique chez la femme enceinte, le diagnostic repose en premier sur le sérodiagnostic qui doit être pratiqué au cours du premier trimestre.
Soit le premier séro diagnostic est négatif (IgG négatif, IgM négatif), la femme non protégée ; il faut faire un sérodiagnostic tout les mois, le dernier sur sang maternel au moment de l'accouchement ou trois à quatre semaines après l'accouchement.
S'il se positive au cours de la grossesse, c'est une séro conversion : le diagnostic de toxoplasmose acquise au cours de la grossesse est certain. Il faut dater l'infection et faire des examens complémentaires en fonction de l'âge de la grossesse.
Plus délicat, en cas de présence IgG et d'IgM lors de la première sérologie. La datation de la contamination repose alors sur la cinétique des anticorps et l'avidité des IgG. Le présence d'une forte avidité (supérieure à 30 %) signe une toxoplasmose acquise depuis plus de 4 mois (donc avant la grossesse). Il est inutile de répéter les examens et on peut rassurer la patiente.
La faible avidité des IgG ne signifie pas que la toxoplasmose date de moins de quatre mois. Il faut refaire un nouveau sérodiagnostic et si le taux des IgG double que l'on peut poser le diagnostic de toxoplasmose acquise au cours de la grossesse. Le début de l'infection remonte deux mois avant le prélèvement Si le taux reste stable, c'est une toxoplamose acquise avant la grossesse.
La présence d'IgG seule sans IgM ne nécessite aucun contrôle supplémentaire.
La présence d'IgM seule sans IgG est le plus souvent en rapport avec des IgM non spécifique. Cependant il faut savoir que si les IgM sont le signe d'une infection récente (ils apparaissent en quelques jours, le pic est atteint en 2 - 3 mois et ils diminuent), ils peuvent persister plusieurs mois, voire plusieurs années ; plus d'un quart des individus gardent des IgM anti-toxoplasmiques plus de 2 ans.
Dès la séroconversion prouvée, la femme est mise sous spiramycine à la dose de 3 grammes trois fois par jour et jusqu'à la réalisation de l'amniocentèse. En cas de présence d'IGM, au cours du premier prélèvement, on peut mettre la femme sous spiramycine en attendant le deuxième prélèvement.
Faire le diagnostic de toxoplasmose congénitale au cours de la grossesse
Repose sur la recherche de toxoplasme dans le liquide amniotique par amniocentèse (la ponction fœtale est désuet) et la recherche mensuelle de signes à l'échographie et éventuellement par IRM.
Amniocentèse
Recherche de toxoplasme par PCR. Cette amniocentèse sera effectué systématiquement pour toute séro conversion avant 22 semaines mais pas avant 18 semaines et après un délai de quatre à six semaines entre l'infection maternelle. La quantification du nombre de copie de PCR est un élément pronostic, la présence de plus de 100 copies par millilitre est un facteur de mauvis pronostic. Il n'existe pas de faux positif mais la valeur prédictive négative est de 87 % ce qui veut dire qu'une fois sur dix la parasite est présent mais la PCR ne le détecte pas. La quantité de liquide amniotique prélevée est très importante, il faut au minimum 20 millilitres.
Aspect échographique : dépendant du terme de l'infection
Il est important de noter que des symptômes échographiques peuvent être absents alors que le fœtus est infecté : en effet, près de 80% des fœtus infectés au premier trimestre seront symptomatiques à l'échographie, 20% au deuxième trimestre et aucun si l'infection a eu lieu au troisième trimestre.
Au niveau du cerveau fœtal, on peut voir :
- une dilatation des ventricules latéraux débutant par les cornes occipitales, rapidement évolutive, bilatérale si sténose de l'aqueduc de Sylvius ou unilatérale si sténose du trou de Monro. Mais l'absence de dilatation n'a pas une bonne valeur prédictive négative car existence d'atteinte sévère même en l'absence de d'envahissement de l'aqueduc de Sylvius (porencéphalie ou polymicrogyrie) ;
- des hyperdensités qui sont souvent mieux vues par la voie endovaginale (haute fréquence) de pronostic incertain mais souvent en rapport avec la choriorétinite.
Autres signes :
- épanchement péricardique et ascite, calcifications hépatiques, hyperéchogénicité intestinale ou placentamégalie ou placentite.
Aspects par IRM
Pas d 'IRM avant 28 semaines soit pas avant le début de l'apparition de la scissure de Rolando ++ ou mieux 32 semaines. Confirme l'atteinte multifoccale et recherche d'anomalie de la gyration type polymicrogyrie
Traitement et surveillance de la toxoplasmose au cours de la grossesse
Selon les préconisations de l'OMS :
Si la PCR est négative
On continue la spiramycine jusqu'à l'accouchement et on réalise une échographie une fois par mois. La recherche d'une toxoplasmose congénitale sera fait sur le nouveau né par le dosage des IgG et des IgM du nouveau-né.
Si la PCR est positive
La spiramycine est remplacée par la pyriméthanine 50 mg par jour (Malocide©) et du sulfadiazine (Adiazine©) 1,5 grammes deux fois par jour associée avec de l'acide folinique (Lederfoline©) 50 mg une fois par semaine. La surveillance échographique se fera toutes les deux semaines et une surveillance de la toxicité des médicaments assurée par une numération formule sanguine une fois par semaine ; la pyrimethamine entraîne une carence en acide folique avec anémie mégaloblastique, et parfois granulopénie et thrombopénie. La sulfadiazine s'accompagne d’un risque grave d'allergie cutanée et de thrombopénie, anémie hémolytique immuno-allergique, aplasie médullaire.
En 2007 est parue une méta-analyse de différentes études de cohortes ; cette étude montre que le traitement préventif de la transmission en cours de grossesse n'est efficace que s'il est prescrit moins de trois semaines après la séroconversion et que les traitements curatifs (en cas de suspicion d'atteinte fœtale) ne semblent pas diminuer le risque d'atteinte fœtale.
À la naissance : faire le diagnostic de toxoplasmose congénitale chez le nouveau né
Le diagnostic de la toxoplasmose congénitale se fait chez les enfants avec une PCR négative au cours de l'amniocentèse ou dans les séroconversions du troisième trimestre n'ayant pas subi une amniocentèse.
- Recherche des IgM au sang du cordon : si le dosage est négatif, la cinétique des IgG permettra de faire le diagnostic de toxoplasmose congénitale. Il faut vérifier la baisse du taux des IgG dont la demie vie est de 3 semaines tout arrêt ou réascencion de la décroissance des IgG signe la toxoplasmose congénitale.
- Recherche des IgM au sang du cordon : IgM est positif, il faut refaire 72 heures après une recherche des IgM dans le sang périphérique du nouveau-né pour éliminer les quelques cas de transmission d'IgM maternelle au cours de l'accouchement. Si celle-ci est positive le diagnostic de toxoplasmose congénitale est confirmée. Si celle-ci est négative on se retrouve dans le schéma ci dessous
Le nouveau né bénéficiera d'une échographie transfontanellaire et d'un examen ophtalmologique.
Traitement de la toxoplasmose congénitale chez le nouveau né
C'est l'association de pyriméthanine 1 mg/kg/j pendant 2 mois puis 0,5 mg/kg/j pendant 10 mois (Malocide©) avec de la sulfadiazine (Adiazine ©) 100 mg/kg/j pendant un an associé avec de l'acide folinique (Folinoral 25 ©) 25 mg fois par semaine. La recherche d'une toxicité sanguine du traitement sera faite. La surveillance ophtalmologique devra durer plusieurs années.
Pronostic
Les deux critères de pronostics les plus sûrs sont la charge en toxoplasme dans le liquide amniotique et le terme de l'infection toxoplasmique : avant 20 semaines et surtout avant 10 semaines. La probabilité de retrouver des signes échographiques après une séro conversion supérieure à 24 semaines est inférieure à 5 %. Si une infection survient avant 10 semaines, il est possible d'avoir un bon pronostic avec le traitement (pyriméthanine 50 mg par jour (Malocide©) + sulfadiazine (Adiazine ©) 1,5 grammes deux fois par jour) mais il faut bien avertir les parents sur l'incertitude du pronostic neurologique et oculaire. L'IMG est acceptée à la demande des parents. Le risque de choriorétinite serait augmenté si il y a plus de 8 semaines entre la séroconversion et le début du traitement et par la présence de zone hyperdense cérébrale à l'échographie. Bien entendu devant tout signe de dilatation ventriculaire l'échographie, l'IMG est acceptée à la demande des parents.
En 1995, le rapport de l'AFSSAPS évalue à 600, en France, le nombre de naissances d'enfants porteurs d'une toxoplasmose congénitale ; 174 ont des séquelles dont 11 à type d'hydrocéphalie, les autres étant porteurs d'une choriorétinite.
Prophylaxie pour la femme enceinte
La vaccination n'existant pas, la prévention est le meilleur traitement :
- ne consommer que de la viande bien cuite (cuisson à plus de 67 °C au cœur des viandes), surtout le mouton ;
- lavage approfondi des salades et crudités, nettoyage des surfaces de travail ayant servir à préparer les légumes ;
- éviter de manger à l'extérieur des légumes dont on ne connaît pas la préparation ;
- porter des gants en cas de jardinage ou si vous vous occupez de la litière d'un chat et se laver les mains ;
- ne pas s'occuper de la litière d'un chat ou la nettoyer avec de l'eau bouillante, mais bien entendu le chat peut se mettre sur vous et vous pouvez le caresser ! Le risque est quasiment nul si le chat n'a pas accès à l'extérieur et qu'il ne mange pas de viande crue ;
- laver (et peler) les fruits et légumes avant de les consommer, avec de l'eau vinaigrée ; cuisson d'au moins une minute à 60 °C pour les végétaux.
Les précautions suivantes ont une efficacité incertaine sur la destruction des toxoplasmes :
- la congélation : des oocytes sporulés ont été retrouvés 28 jours après une congélation à -21 °C ;
- salaison, condiments, fumaison, saumure, conservation sous vide, dessiccation, lyophilisation, désinfection par ultra-violets ou infrarouges, cuisson par micro-ondes (voir Conservation des aliments).
Toxoplasmose de l’immunodéprimé
Deux cas peuvent se présenter, selon que le déficit immunitaire est acquis ou provoqué par des médicaments. Ces cas influent sur la manière dont la contamination survient et sur ses signes cliniques.
Déficit immunitaire acquis (cas du SIDA)
On décrit de rares cas où un sujet VIH+, sans immunité anti-toxoplasmique (pas de contact antérieur) contracte une toxoplasmose, mais le plus souvent il s'agit de patients immunisés contre la toxoplasmose, donc porteurs de kystes qui réactivent l'infection lors d'une baisse conséquente de leurs défenses immunitaires ; généralement, ils présentent une toxoplasmose cérébrale.
La toxoplasmose cérébrale est une maladie opportuniste dont la survenue chez les personnes séropositives marque l'évolution de l'infection à VIH au stade de sida. Elle survient en règle générale chez des sujets séropositifs au VIH, ayant moins de 200 lymphocytes T CD4+, avec une sérologie toxoplasmique positive et ne recevant pas de prophylaxie spécifique. C'est alors que les bradyzoïtes libèrent les tachyzoïtes qui essaiment dans tout le corps via le système sanguin. En 2008 en France, la toxoplasmose cérébrale représentait 12 % des personnes qui découvraient leur séropositivité au VIH après le déclenchement d'une affection opportuniste.
Les symptômes de début peuvent être insidieux, céphalées d'installation récente ou réactivation de céphalées anciennes, avec ou sans fièvre. Trois situations sont possibles :
- il s'agit d'un (ou de plusieurs) abcès cérébral (cas le plus fréquent) donnant un tableau neurologique rapidement progressif. Les signes cliniques dépendent de la localisation de(s) l'abcès : hémiplégie ou hémiparésie, syndrome cérebelleux, aphasie, amputation du champ visuel, ou signes plus diffus à type de somnolence, désorientation, crises comitiales ;
- il s'agit d'un abcès médullaire (rare) donnant un tableau paraparétique ou paraplégique associé à des troubles sensitifs et/ou sphinctériens ;
- il s'agit d'une encéphalite toxoplasmique, plus fréquente chez les transplantés que chez les patients VIH.
Traitements curatifs
L'association de pyriméthamine (Malocide®), de sulfadiazine (Adiazine®) et d'acide folinique (pour la prévention des effets hématotoxiques) pendant 6 semaines est le traitement de référence. On utilise aussi en alternative le cotrimoxazole (Bactrime®) ou l'atovaquone (Wellvone®). Une attention particulière doit être portée aux intractions avec les antirétroviraux.
Traitements préventifs
La prophylaxie est recommandée en cas de présence d'anticorps anti-Toxoplasma gondii et si les lymphocytes CD4 sont inférieurs à 100 par mm³ de sang. Une association de pyriméthamine, sulfadiazine et acide folinique est recommandée. Le cotrimaxozole peut aussi être utilisé avec l'avantage d'être aussi efficace pour la prophylaxie de la pneumocystose, autre maladie opportuniste du SIDA en association fréquente.
Déficit immunitaire provoqué (cas des transplantés et des greffés)
Il peut s'agir ici soit de la réactivation de kystes résultant d'une contamination passée du receveur (par exemple lors d'une greffe de moelle osseuse), soit de l'introduction chez le receveur de kystes contenus dans le greffon (par exemple lors d'une greffe du cœur).
Au plan clinique, les manifestations dans ce cas sont celles d'une toxoplasmose aiguë disséminée.
Dans tous les cas où l'on s'apprête à provoquer un déficit immunitaire, il faut connaître si possible le statut immunitaire du patient vis-à-vis de la toxoplasmose avant la mise en place du traitement immunosuppresseur. De plus, il est indispensable de mettre en place une surveillance du patient ainsi que de suivre des mesures prophylactiques rigoureuses.
Professions à risque
Les professionnels en contact avec de la viande crue, les animaux ou les selles de félins contaminés, voire des objets portant le germe sont les plus exposés. Le risque est donc présent pour :
- les vétérinaires, éleveurs, gardiens d'animaux (félins) et assistants ;
- les employés d'abattoirs, de boucherie, de cuisine, les personnes préparant ou inspectant de la viande ;
- les agriculteurs ;
- les paysagistes, les jardiniers ;
- les laborantins ;
- les professionnels de santé en général ;
- les archéologues.
Précautions à prendre
Gardiens, éleveurs d'animaux
Il convient d'éliminer systématiquement les excréments des félins, de jeter la litière sèche sans la secouer. La destruction peut se faire par dépôt en décharge, incinération, ou en les enterrant à une bonne profondeur.
Les bacs ou plateaux de litière doivent être désinfectés (par étuvage à 70 °C pendant 10 minutes au moins) chaque jour, de même que les pelles, balais et autre articles de nettoyage. Les accessoires de nettoyage doivent être conservés dans la même zone que les animaux. Le port de gants de protection jetables est recommandé pour manier la litière et pour travailler dans un sol où il peut y avoir des excréments de félins. Les mains doivent être lavées après avoir enlevé les gants.
Les félins doivent être tenus à l'écart des autres animaux pour éviter les risques de contamination. Il ne faut pas donner de viande crue aux félins, sauf si elle a été congelée plus de 24h.
Personnes en contact avec de la viande crue
Les mains doivent être abondamment lavées avec de l'eau et du savon, en utilisant des lavabos ou des éviers à commande fémorale. Il ne faut pas se toucher la bouche ou les yeux après avoir manipulé de la viande crue. Les surfaces et les outils utilisés (comptoirs, couteaux, machines...) doivent être nettoyées à l'eau savonneuse.
Ne pas laisser les insectes (blattes notamment) entrer en contact avec les aliments et les zones de préparation car ils pourraient amener des oocystes.
Agriculteurs, paysagistes, jardiniers
La terre peut être une source de contamination, en particulier aux endroits fréquentés par les chats (les excréments de chat sont fréquemment présents dans les sols). Il convient donc de bien se laver les mains après avoir travaillé la terre ou touché des animaux, le port de gants étant recommandé. Le port de gants ne doit pas dispenser de se laver les mains ensuite. En cas d'avortement d'une femelle, il ne faut pas toucher l'embryon à mains nues. Il doit être confié à un laboratoire avec des spécimens de sang et de placenta pour connaître son statut vis-à-vis du parasite. Ce qui subsiste doit être enterré à bonne profondeur ou être brûlé, en prenant soin de ne pas laisser d'animaux (chats, chiens, rongeurs) y accéder.
Les chats doivent être tenus à l'écart du fourrage, leurs excréments doivent en être éliminés. Les chats adultes ont plus de chances d'avoir déjà développé une résistance à la toxoplasmose ; on peut les laisser pénétrer dans les granges. Pour réduire le risque de propagation, il vaut mieux éviter les contacts avec les chats errants.
Personnels de laboratoire
Il est conseillé aux femmes enceintes de ne pas travailler sur des échantillons soumis pour analyse de Toxoplasma gondii.
L'exposition à des substances contaminées nécessite le port de vêtements de protection adaptés. Un vêtement souillé doit être identifié par un logo de risque biologique ; il doit être lavé selon les méthodes de désinfection requises.
La production et l'exposition à des aérosols de tissus animaux est fortement déconseillée.
Professionnels de la santé
Il n'a pas été démontré que la toxoplasmose pouvait être transmise par l'urine ou les selles humaines contaminées. Cependant, il vaut toujours mieux porter des gants jetables pour travailler avec des personnes atteintes d'incontinence. Les mains et les ongles doivent être soigneusement lavés avec de l'eau savonneuse après avoir retiré les gants.