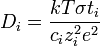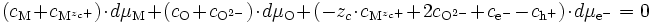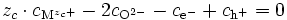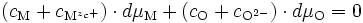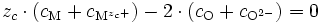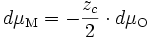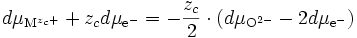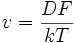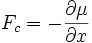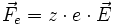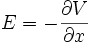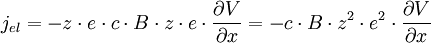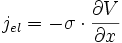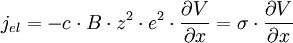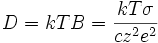Théorie de la cinétique d'oxydation de Wagner - Définition
La liste des auteurs de cet article est disponible ici.
Prérequis
Les prérequis pour cette étude sont :
- la loi de Fick, loi phénoménologique de la diffusion ;
- la loi de Nernst-Einstein, résultant de l'étude statistique du mouvement d'une particule sous l'effet combiné d'une force et de chocs aléatoires ;
- la loi d'Ohm sous sa forme microscopique ;
- la conduction électrique dans les oxydes cristallins
- la relation thermodynamique de Gibbs-Duhem
Équilibre thermodynamique
Dans cette partie, nous considèrerons pour simplifier que la migration, pour le métal ou bien l'oxygène, se fait par une seule espèce (ion interstitiel ou bien lacune, cf. Défaut cristallin et Notation de Kröger et Vink), et nous noterons :
- M pour désigner l'ion métallique en position normale dans l'oxyde MM ;
- Mzc+ pour désigner l'ion mobile dans l'oxyde, c'est-à-dire soit l'ion interstitiel Mizc•, soit la lacune métallique VMzc ' ;
- O pour désigner l'ion oxygène en position normale OO ;
- O2- pour désigner l'ion mobile dans l'oxyde, Oi2 ' ou VO2• ;
- e- pour désigner les électrons libres e' et h+ les trous d'électrons h•.
Notez que lorsqu'une lacune se déplace, cela équivaut globalement au déplacement en sens inverse d'un ion de charge opposée à la charge effective de la lacune.
Si l'on écrit la relation de Gibbs-Duhem, on obtient :
-
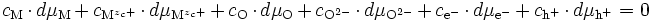
Écrivons maintenant les équilibres chimiques locaux :
- cations : M ⇌ Mzc+ + zc e- ⇒ dμM = dμMzc+ + zc dμe- (E11) ;
- anions : O + 2e- ⇌ O2- ⇒ dμO + 2 dμe- = dμO2- (E12);
- électrons et trous d'électron : Ø ⇌ e- + h+ ⇒ 0 = dμe- + dμh+ soit dμe- = - dμh+ (E13).
La relation de Gibbs-Duhem () s'écrit donc :
L'électroneutralité s'écrit :
donc
Puisque nous sommes proches de la stœchiométrie, on peut écrire la neutralité électrique du cristal : l'ensemble des cations (en position interstitielle ou en position normale) contrebalance l'ensemble des anions (en position interstitielle ou en position normale) en ce qui concerne les charges :
La relation de Gibbs-Duhem devient donc au final
ou bien encore
et donc
-
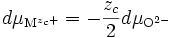
Migration sous l'effet d'un champ
Les espèces effectuant des sauts aléatoires, nous considérons le parcours moyen <X> d'une particule (atome, ion, électron libre, trou d'électron) pendant une durée τ. On peut définir la vitesse moyenne v comme étant
Si la particule est soumise à une force F, alors on peut relier la vitesse moyenne à la force et au coefficient de diffusion D par la loi de Nernst-Einstein :
k étant la constante de Boltzmann et T la température absolue. Si l'on prend la comparaison avec le frottement fluide (freinage du parachute), on peut écrire que la vitesse est proportionnelle à la force :
- v = B⋅F
B étant la mobilité (Beweglichkeit) de l'espèce. On a donc la relation d'Einstein :
- D = B⋅k⋅T (E4)
Le flux j, lui, résulte du mouvement sous l'effet de la force, qui tend à faire migrer les espèces et donc à créer un gradient de concentration, et de l'agitation thermique qui tend elle au contraire à uniformiser la concentration (loi de Fick). Comme on se place dans le cas d'un oxyde dont la composition est proche de la stœchiométrie, on suppose également que la variation de concentration est faible. Le flux peut donc s'écrire, par approximation :
- j = v⋅c = c⋅B⋅F (E5)
c étant la concentration.
Potentiel chimique
La force Fc résultant du potentiel chimique μ peut s'écrire, à une dimension :
et donc () devient :
-
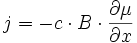
Champ électrique
Si une particule porte z charges élémentaires e, alors elle subit la force Fe (force électrostatique ou force de Coulomb) :
Le champ électrique E dérive d'un potentiel V, ce qui s'écrit à une dimension :
d'où, d'après (), un flux :
-
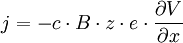
soit une densité de courant électrique (flux de charges) jel valant d'après ()
On peut faire un parallèle avec le loi d'Ohm reliant cette densité de courant électrique jel au gradient de potentiel :
σ étant la conductivité électrique. On a donc :
soit
- σ = c⋅B⋅z²⋅e² (E8)
et donc d'après la relation d'Einstein () :
Lorsqu'il y a plusieurs porteurs de charge i, la conductivité totale σ est la somme des conductivités pour chaque espèce σi :
- σ = ∑i σi
On peut aussi écrire que chaque σi est une portion ti de σ :
- σi = ti⋅σ
avec évidemment
- ∑i = ti = 1
Le coefficient ti est appelé le « nombre de transport » de l'espèce i.
On obtient donc pour une espèce donnée :
-