Tableau périodique des éléments - Définition
La liste des auteurs de cet article est disponible ici.
Présentations alternatives
De très nombreuses présentations alternatives du tableau périodique ont été proposées tout au long du XXe siècle, et des présentations graphiques innovantes sont encore régulièrement proposées. L'une des plus anciennes et des plus simples est celle d'un autodidacte français par ailleurs inconnu, Charles Janet, qui a donné son nom à une disposition du tableau élaborée au début du XXe siècle et récemment redécouverte par les Anglo-saxons, chez lesquels elle est assez bien connue des spécialistes du sujet (sous les noms de Janet Form ou de Left-Step Periodic Table) car elle a le double mérite de rester familière et de disposer les éléments dans l'ordre naturel des blocs (de droite à gauche), à la différence du tableau usuel :
| f1 | f2 | f3 | f4 | f5 | f6 | f7 | f8 | f9 | f10 | f11 | f12 | f13 | f14 | d1 | d2 | d3 | d4 | d5 | d6 | d7 | d8 | d9 | d10 | p1 | p2 | p3 | p4 | p5 | p6 | s1 | s2 |
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | ||||||||||||||||||||||||||||||
| B | C | N | O | F | Ne | Na | Mg | ||||||||||||||||||||||||
| Al | Si | P | S | Cl | Ar | K | Ca | ||||||||||||||||||||||||
| Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | Rb | Sr | ||||||||||||||
| Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | Cs | Ba | ||||||||||||||
| La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | Fr | Ra |
| Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Uuq | Uup | Uuh | Uus | Uuo | Uue | Ubn |
| Tableau périodique organisé à la façon de Charles Janet. | |||||||||||||||||||||||||||||||
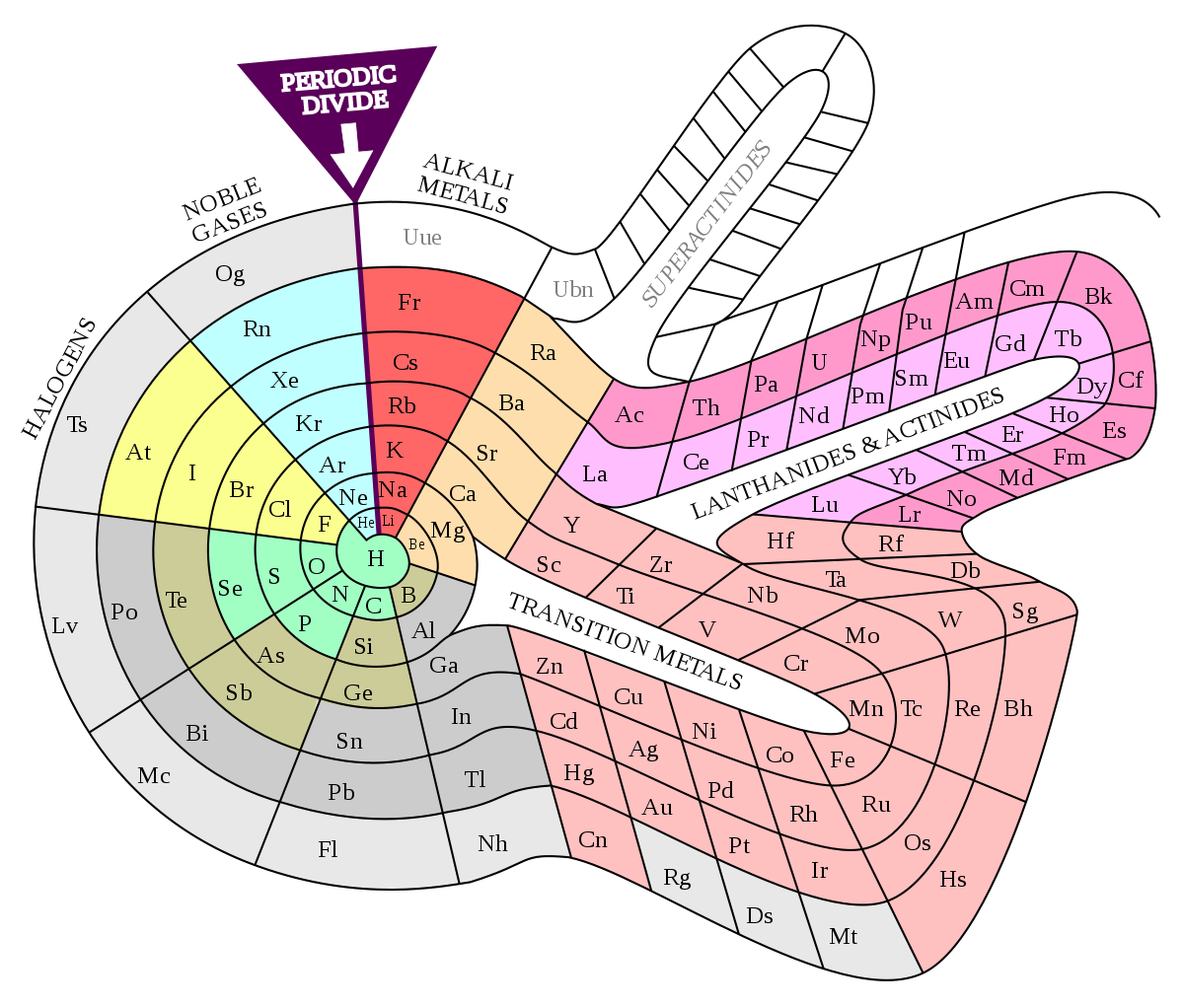
Une autre représentation est celle de Theodor Benfey, datée de 1960, dont l'objectif était de remédier aux discontinuités du tableau standard à l'aide d'une représentation en spirale :
De nombreux modèles en trois dimensions ont également été proposés afin d'enrichir la représentation des éléments par diverses informations spécifiques, qu'on peut retrouver en suivant ce lien très complet.
Historique
De la toute première tentative de classification des éléments chimiques par Antoine Lavoisier en 1789 au tableau périodique de Glenn Seaborg que nous utilisons aujourd'hui, de nombreux hommes de sciences, issus d'horizons — et parfois de disciplines — différents, ont apporté chacun leur contribution, sur une période de près de deux siècles.
Première classification d'Antoine Lavoisier
C'est en 1789 que le chimiste français Antoine Lavoisier a publié à Paris son Traité élémentaire de chimie, présenté dans un ordre nouveau et d'après les découvertes modernes. Cet ouvrage en deux volumes a jeté les bases de la chimie moderne, en faisant le point sur les connaissances de la fin du XVIIIe siècle dans cette discipline. Il y précise notamment le concept d'élément chimique comme une substance simple qui ne peut être décomposée en d'autres substances, avec en corollaire la loi fondamentale de conservation de la masse de chacune de ces substances simples au cours des réactions chimiques. Il mentionna également le fait que de nombreuses substances considérées comme simples par le passé se sont révélées être en réalité des composés chimiques (par exemple l'huile et le sel marin), et il précisa s'attendre à ce qu'on considère sous peu les terres (c'est-à-dire certains minerais) comme des substances composées de nouveaux éléments.
Il publia dans cet ouvrage un tableau récapitulatif des « substances » considérées à son époque comme des éléments chimiques, en prenant soin d'établir une équivalence avec le vocabulaire hérité des alchimistes afin d'éliminer toute ambiguïté. Ce tableau, qui se voulait exhaustif et outil de référence, mentionnait ainsi, parmi les éléments chimiques, la lumière et le feu, encore considérés à cette époque comme des principes « chimiques » bien que Lavoisier lui-même ait invalidé la théorie du phlogistique :
| Noms nouveaux | Noms anciens correspondants | |
| Substances simples qui appartiennent aux trois règnes et qu'on peut regarder comme les éléments des corps | Lumière | |
| Calorique | Chaleur | |
| Oxygène | Air déphlogistiqué | |
| Azote | Gaz phlogistiqué | |
| Hydrogène | Gaz inflammable | |
| Substances simples non-métalliques oxydables et acidifiables | Soufre | |
| Phosphore | ||
| Carbone | Charbon pur | |
| Radical muriatique | Inconnu | |
| Radical fluorique | Inconnu | |
| Radical boracique | Inconnu | |
| Substances simples métalliques oxydables et acidifiables | Antimoine | |
| Argent | ||
| Arsenic | ||
| Bismuth | ||
| Cobalt | ||
| Cuivre | ||
| Étain | ||
| Fer | ||
| Manganèse | ||
| Mercure | ||
| Molybdène | ||
| Nickel | ||
| Or | ||
| Platine | ||
| Plomb | ||
| Tungstène | ||
| Zinc | ||
| Substances simples salifiables terreuses | Chaux | |
| Magnésie | Magnésie | |
| Barite | Barote | |
| Alumine | Argile | |
| Silice | Terre siliceuse | |
| « Tableau des substances simples » publié par Antoine Lavoisier en 1789. | ||
Les éléments chimiques y sont classés en quatre familles :
-
- Les éléments impondérables (gaz et autres « essences »)
- Les non-métaux
- Les métaux
- Les « terres », à savoir des minerais (oxydes, sulfates) considérés comme corps simples.
Le chlore est désigné comme « radical muriatique », car Lavoisier considérait que tous les acides étaient des oxoacides — le nom oxygène signifie étymologiquement « formant des acides » — et cherchait donc le « radical » que l'oxygène aurait rendu acide — l'acide muriatique désignait l'acide chlorhydrique, qui ne contient cependant pas d'oxygène.
Cette classification a surtout le mérite de clarifier certaines notions fondamentales, mais ne révèle encore aucune périodicité des propriétés des éléments classés : les métaux sont ainsi recensés tout simplement par ordre alphabétique en français.
Triades de Johann Döbereiner
La première tentative de classification moderne des éléments chimiques revient au chimiste allemand Johann Wolfgang Döbereiner qui, en 1817, nota que la masse atomique du strontium (88) était égale à la moyenne arithmétique des masses atomiques du calcium (40) et du baryum (137), qui ont des propriétés chimiques semblables (aujourd'hui, ils sont classés parmi les métaux alcalino-terreux). En 1829, il avait découvert deux autres « triades » de ce type : celle des halogènes (la masse atomique du brome (80) étant égale à la moyenne arithmétique (81) de celles du chlore (35,5) et de l'iode (127)) et celle des métaux alcalins (la masse atomique du sodium (23) étant égale à la moyenne arithmétique de celles du lithium (7) et du potassium (39)).
D'autres chimistes identifièrent d'autres séries d'éléments, et Leopold Gmelin publia en 1843 la première édition de son Handbuch der Chemie, qui mentionnait des triades, ainsi que trois « tétrades » et une « pentade » — azote, phosphore, arsenic, antimoine et bismuth, que nous connaissons aujourd'hui comme les éléments du groupe 15.
Tétrades de Jean-Baptiste Dumas
En 1859, le chimiste français Jean-Baptiste Dumas généralisa les triades de Döbereiner en les étendant en tétrades incluant les éléments les plus légers, définies non plus par les moyennes arithmétiques, mais par une progression similaire d'une tétrade à l'autre, par exemple :
Bien qu'en apparence similaire à celle de Döbereiner, l'approche de Dumas était potentiellement bien plus féconde car applicable de façon pertinente à un bien plus grand nombre d'éléments : alors que les progressions arithmétiques sont restreintes à quelques groupes d'éléments, l'incrément constaté par Dumas entre éléments successifs aux propriétés similaires mesure précisément la longueur de la période qui sépare ces deux éléments — incrément d'environ 16 entre les deux premiers éléments d'une tétrade, puis incrément d'environ 48 entre deuxième et troisième éléments, puis entre troisième et quatrième éléments.
Vis tellurique de Chancourtois
Le premier à remarquer la périodicité des propriétés chimiques des éléments fut le géologue français Alexandre-Émile Béguyer de Chancourtois lorsqu'il classa en 1862 les éléments chimiques alors connus en fonction de leur masse atomique déterminée en 1858 par le chimiste italien Stanislao Cannizzaro. Il normalisa la masse atomique de tous les éléments en prenant celle de l'oxygène égale à 16, et, considérant que « les propriétés des éléments sont les propriétés des nombres, » organisa les éléments chimiques en spirale sur un cylindre divisé en seize parties, de telle sorte que les éléments aux propriétés similaires apparaissent l'un au-dessus de l'autre.
Chancourtois remarqua alors que certaines « triades » se retrouvaient précisément alignées dans cette représentation, ainsi que la tétrade oxygène – soufre – sélénium – tellure, qui se trouvait également avoir des masses atomiques à peu près multiples de seize (respectivement 16, 32, 79 et 128). C'est la raison pour laquelle il appela cette représentation « vis tellurique, » en référence au tellure. C'était la première ébauche de classification périodique des éléments. Celle-ci ne retint cependant pas l'attention de la communauté scientifique, car Chancourtois n'était pas chimiste et avait employé des termes appartenant plutôt au domaine de la géochimie dans la publication qu'il avait adressée à l'Académie des sciences, laquelle fut éditée de surcroît sans ses schémas explicatifs, ce qui rendit le texte abscons.
D'un point de vue conceptuel, c'était une grande avancée, mais, d'un point de vue pratique, Chancourtois n'avait pas identifié la période correcte pour les éléments les plus lourds, de sorte que, dans sa représentation, une même colonne regroupait le bore, l'aluminium et le nickel, ce qui est correct pour les deux premiers mais totalement erroné d'un point de vue chimique pour le troisième.
Loi des octaves de John Newlands
Dans la foulée, le chimiste anglais John Alexander Reina Newlands publia en 1863 une classification périodique qui eut, elle, un plus fort retentissement (quoique tardif, et a posteriori), car il avait organisé les premiers éléments alors connus par masse atomique croissante — plus précisément, par masse équivalente croissante — dans un tableau à sept lignes en les arrangeant de telle sorte que leurs propriétés chimiques soient similaires par lignes, sans hésiter à placer deux éléments dans une même case si nécessaire pour éviter de laisser des cases vides par ailleurs.
Ce faisant, il avait identifié une nouvelle triade, dont les extrémités étaient le silicium et l'étain, et dont l'élément médian restait à découvrir : il prédit ainsi l'existence du germanium, en lui assignant une masse atomique d'environ 73. Mais la grande faiblesse de son travail était qu'il n'avait pas laissé de case vide dans son tableau pour accueillir notamment le futur germanium : il avait en fait cherché avant tout à classer les éléments connus dans un tableau complet sans chercher de classification plus large tenant compte de possibles éléments à découvrir, qu'il avait pourtant pressentis. De plus, comme Chancourtois, il avait un problème de périodicité, car si les éléments légers connus à l'époque avaient bien une périodicité chimique tous les sept éléments, cela cessait d'être valable au-delà du calcium, et le tableau de Newlands s'avère alors inopérant :
| I. | II. | III. | IV. | V. | VI. | VII. | VIII. | |
| 1 | H | F | Cl | Co & Ni | Br | Pd | I | Pt & Ir |
| 2 | Li | Na | K | Cu | Rb | Ag | Cs | Tl |
| 3 | Be | Mg | Ca | Zn | Sr | Cd | Ba & V | Pb |
| 4 | B | Al | Cr | Y | Ce & La | U | Ta | Th |
| 5 | C | Si | Ti | In | Zr | Sn | W | Hg |
| 6 | N | P | Mn | As | Di & Mo | Sb | Nb | Bi |
| 7 | O | S | Fe | Se | Rh & Ru | Te | Au | Os |
| Tableau de John Newlands illustrant la « loi des octaves », 1865. | ||||||||
La mise en évidence d'une périodicité globale jusqu'au calcium était néanmoins une grande avancée, et Newlands présenta cette classification en l'appelant « loi des octaves » par analogie avec les sept notes de musique, mais ce travail fut assez mal accueilli par ses pairs de la Société de chimie de Londres, qui le tournèrent souvent en ridicule et firent obstacle à sa publication ; ce n'est qu'après la publication des travaux de Dimitri Mendeleïev que la qualité de cette analyse a été reconnue.
Notation d'éléments manquants par William Odling
Le chimiste anglais William Odling — secrétaire de la Société de chimie de Londres, et donc rival de Newlands — travaillait également, dans les années 1860, sur une table périodique des éléments chimiques remarquablement proche de celle que publierait Mendeleïev en 1869. Elle était organisée en périodes verticales avec des cases vides pour les éléments manquants et plaçait — à la différence du premier tableau de Mendeleïev — le platine, le mercure, le thallium et le plomb dans les bons groupes. Son action négative à l'encontre de Newlands entacha néanmoins définitivement la renommée d'Odling, et sa contribution à l'élaboration du tableau périodique des éléments est aujourd'hui largement méconnue.
Introduction de la valence avec Lothar Meyer
La contribution du chimiste allemand Lothar Meyer est à peine mieux reconnue que celle d'Odling, car ses travaux décisifs ont été publiés après ceux de Mendeleïev alors qu'ils étaient pour la plupart antérieurs. Il publia ainsi une première version de sa classification des éléments en 1864, puis finalisa en 1868 une seconde version plus aboutie qui ne fut intégralement publiée qu'à sa mort, en 1895.
Le premier tableau de Meyer comprenait vingt-huit éléments classés en six familles définies par leur valence : c'était un grand pas en direction de la forme moderne du tableau périodique, organisé en groupes dépendant de la configuration électronique des éléments, elle-même directement en relation avec leur valence ; ce n'était néanmoins pas encore le même tableau qu'aujourd'hui, car les éléments étaient toujours rangés par masse atomique croissante. Le second tableau de Meyer, qui élargissait et corrigeait le premier, fut publié en 1870, quelques mois après celui de Mendeleïev, dont il renforça l'impact sur la communauté scientifique en apportant aux thèses du chimiste russe, encore très contestées, le soutien de travaux indépendants. La grande force de ce travail résidait dans les périodes de longueur variable, avec une disposition des éléments qui permettait d'éviter les regroupemets fâcheux de Newlands, tels que le fer, l'or et certains éléments du groupe du platine parmi l'oxygène, le soufre, et les autres éléments du groupe 16 :
| I. | II. | III. | IV. | V. | VI. | VII. | VIII. | IX. |
| B = 11,0 | Al = 27,3 | ? | ?In = 113,4 | Tl = 202,7 | ||||
| ? | ? | ? | ||||||
| C = 11,97 | Si = 28 | ? | Sn = 117,8 | Pb = 206,4 | ||||
| Ti = 48 | Zr = 89,7 | ? | ||||||
| N = 14,01 | P = 30,9 | As = 74,9 | Sb = 122,1 | Bi = 207,9 | ||||
| V = 51,2 | Nb = 93,7 | Ta = 182,2 | ||||||
| O = 15,96 | S = 31,98 | Se = 78 | Te = 128? | ? | ||||
| Cr = 54,4 | Mo = 95,6 | W = 183,5 | ||||||
| ? | F = 19,1 | Cl = 35,38 | Br = 79,75 | I = 126,5 | ? | |||
| Mn = 54,8 | Ru = 103,5 | Os = 198,6 | ||||||
| Fe = 55,9 | Rh = 104,1 | Ir = 196,7 | ||||||
| Co = Ni = 58,6 | Pd = 106,2 | Pt = 196,7 | ||||||
| Li = 7,01 | Na = 22,99 | K = 39,04 | Rb = 85,2 | Cs = 132,7 | ? | |||
| Cu = 63,3 | Ag = 107,66 | Au = 196,2 | ||||||
| ?Be = 9,3 | Mg = 23,9 | Ca = 39,9 | Sr = 87,0 | Ba = 136,8 | ? | |||
| Zn = 64,9 | Cd = 116,6 | Hg = 199,8 | ||||||
| Tableau périodique des éléments chimiques de Lothar Meyer, publié en 1870. | ||||||||
Meyer avait également remarqué que si l'on trace une courbe représentant en abscisse la masse atomique et en ordonnée le volume atomique de chaque élément, cette courbe présente une série de maxima et de minima périodiques, les maxima correspondant aux éléments les plus électropositifs.
Classification périodique de Mendeleïev
Malgré la qualité réelle des travaux de ses contemporains, c'est bien au chimiste russe Dimitri Ivanovich Mendeleïev qu'on doit le premier tableau périodique des éléments s'approchant de celui que nous utilisons aujourd'hui, non seulement dans sa forme mais surtout par la vision qui l'accompagne. À la différence de ses prédécesseurs, Mendeleïev a en effet formulé explicitement en quoi son tableau constituait un outil d'analyse théorique des propriétés de la matière :
- Les éléments chimiques, lorsqu'ils sont ordonnés par masse atomique croissante, montrent une périodicité de leur propriétés chimiques.
- Les éléments qui ont des propriétés chimiques semblables ont ou bien des masses atomiques semblables (osmium, iridium, platine par exemple) ou bien des masses atomiques croissant de façon arithmétique (potassium, rubidium, césium par exemple).
- La disposition des éléments ou des groupes d'éléments dans la table par masse atomique croissante correspond à leur valence et est en rapport, dans une certaine mesure, avec leurs propriétés chimiques.
- Les éléments les plus abondants dans le milieu naturel sont ceux qui ont la plus faible masse atomique.
- La valeur de la masse atomique détermine les propriétés des éléments chimiques.
- La masse atomique de certains éléments devrait parfois être revue, car le tableau est plus cohérent en réarrangeant certains éléments — typiquement, le tellure — sans tenir compte de leur masse atomique expérimentale.
- On doit s'attendre à découvrir des éléments inconnus au moment de la publication de ce tableau, par exemple des éléments analogues à l'aluminium et au silicium, avec une masse atomique comprise entre 65 et 75.
- Il est possible de prédire certaines propriétés des éléments à partir de leur masse atomique.
L'avancée était significative :
-
- Mendeleïv prédit ainsi l'existence d'une série d'éléments, dont il précisa certaines propriétés, à commencer par leur masse atomique :
- l'eka-bore (44), correspondant au scandium (45), découvert en 1879
- l'eka-aluminium (68), correspondant au gallium (69,7), découvert en 1875 — une réussite particulièrement brillante, car Mendeleïev avait prévu une densité de 6 g/cm3 et un bas point de fusion, les valeurs réelles étant 5,9 g/cm3 et 29,78 °C
- l'eka-silicium (72), correspondant au germanium (72,5), découvert en 1882 — là encore, avec un remarquable accord entre les observations et les propriétés physicochimiques prédites par Mendeleïev
- l'eka-manganèse (100), correspondant au technétium (99), découvert en 1937
- Il identifia par sa théorie une dizaine d'éléments dont la masse atomique avait été déterminée de façon incorrecte
- Il réorganisa sans le savoir certains éléments en fonction de leur numéro atomique et non de leur masse atomique
- Mendeleïv prédit ainsi l'existence d'une série d'éléments, dont il précisa certaines propriétés, à commencer par leur masse atomique :
Les travaux de Mendeleïev ont été accueillis avec scepticisme par ses pairs, mais la publication subséquente de plusieurs résultats similaires (ceux de John Newlands et de Lothar Meyer en particulier) obtenus de façon indépendante ont fait basculer le consensus en faveur de cette nouvelle vision des éléments chimiques.
Découverte de l'argon par William Ramsay et Lord Rayleigh
C'est en voulant mesurer avec précision la masse atomique de l'oxygène et de l'azote par rapport à celle de l'hydrogène que John William Strutt Rayleigh nota une divergence entre la masse atomique de l'azote produit à partir d'ammoniac et celle de l'azote séparé de l'air atmosphérique, légèrement plus lourd. Employant une méthodologie rigoureuse, William Ramsay parvint en 1894 à isoler l'argon à partir de « l'azote » atmosphérique, et expliqua l'anomalie apparente de la masse atomique de l'azote atmosphérique en déterminant la masse atomique de ce nouvel élément, pour lequel rien n'était prévu dans le tableau de Mendeleïev. Sa nature gazeuse et son inertie chimique l'avaient rendu jusqu'alors invisible aux chimistes.
La masse atomique de l'argon (un peu moins de 40) est très voisine de celle du calcium (un peu plus de 40) et donc supérieure à celle du potassium (39,1), ce qui posa quelques problèmes de classification car il semblait y avoir « plus de place » dans le tableau périodique entre le chlore et le potassium qu'entre le potassium et le calcium. Les choses se compliquèrent encore lorsque Ramsay et Morris Travers découvrirent le néon en 1898, matérialisant, avec l'hélium (découvert en 1868 par l'astronome français Jules Janssen et l'Anglais Joseph Norman Lockyer), le groupe nouveau des gaz rares (ou gaz nobles), appelé « groupe 0 » : la masse atomique du néon (20,2) était exactement intermédiaire entre celles du fluor (19) et du sodium (23). Ainsi, les gaz rares semblaient se positionner tantôt entre un métal alcalin et un métal alcalino-terreux, tantôt entre un halogène et un métal alcalin.
Rangement par numéro atomique avec Henry Moseley
À la suite de la découverte de l'électron et de celle des isotopes par l'Anglais Joseph John Thomson — qui ont accompagné les débuts de la physique de l'atome avec les travaux de l'Allemand Max Planck, du Néo-Zélandais Ernest Rutherford et du Danois Niels Bohr — les recherches du physicien anglais Henry Moseley sur la corrélation entre la charge du noyau atomique et le spectre aux rayons X des atomes ont abouti en 1913 au classement des éléments chimiques non plus par masse atomique croissante, mais par numéro atomique croissant. C'était une évolution majeure, qui résolvait toutes les inconsistances issues du classement en fonction de la masse atomique, lesquelles devenaient gênantes depuis les travaux de systématisation de Dmitri Mendeleïev.
L'argon était ainsi placé entre le chlore et le potassium, et non plus entre le potassium et le calcium, tandis que le cobalt était clairement positionné avant le nickel bien qu'il soit un peu plus lourd. Il confirma que le tellure devait être placé avant l'iode sans nécessiter de revoir sa masse atomique, contrairement à ce qu'avait suggéré Mendeleïev. Il releva également que les éléments de numéro atomique 43 et 61 manquaient à l'appel : l'élément 43 avait déjà été prédit par Mendeleïev comme eka-manganèse (il s'agit du technétium, radioactif, synthétisé en 1937) mais l'élément 61 était nouveau — il s'agit du prométhium, radioactif également, isolé en 1947 :
| O | I | II | III | IV | V | VI | VII | VIII | |||||||||
| A | B | A | B | A | B | A | B | A | B | A | B | A | B | ||||
| 1 H | |||||||||||||||||
| 2 He | 3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | ||||||||||
| 10 Ne | 11 Na | 12 Mg | 13 Al | 14 Si | 15 P | 16 S | 17 Cl | ||||||||||
| 18 Ar | 19 K | 29 Cu | 20 Ca | 30 Zn | 21 Sc | 31 Ga | 22 Ti | 32 Ge | 23 V | 33 As | 24 Cr | 34 Se | 25 Mn | 35 Br | 26 Fe | 27 Co | 28 Ni |
| 36 Kr | 37 Rb | 47 Ag | 38 Sr | 48 Cd | 39 Y | 49 In | 40 Zr | 50 Sn | 41 Nb | 51 Sb | 42 Mo | 52 Te | (43) | 53 I | 44 Ru | 45 Rh | 46 Pd |
| 54 Xe | 55 Cs | 79 Au | 56 Ba | 80 Hg | 57-71 Ln | 81 Tl | 72 Hf | 82 Pb | 73 Ta | 83 Bi | 74 W | 84 Po | 75 Re | (85) | 76 Os | 77 Ir | 78 Pt |
| 86 Rn | (87) | 88 Ra | 89 Ac | 90 Th | 91 Pa | 92 U | |||||||||||
| 57 La | 58 Ce | 59 Pr | 60 Nd | (61) | 62 Sm | 63 Eu | 64 Gd | 65 Tb | 66 Dy | 67 Ho | 68 Er | 69 Tm | 70 Yb | 71 Lu | |||
| Structure du tableau périodique des éléments publié en 1913 par Henry Moseley. | |||||||||||||||||
Ce tableau, directement inspiré de celui de John Newlands, constituait l'étape intermédiaire conduisant à la disposition contemporaine. En particulier, la numérotation des groupes avec des chiffres romains de I à VIII, qui remontent à Newlands, et les lettres A et B, introduites par Moseley, était encore largement utilisée à la fin du XXe siècle :
| I A | II A | III B | IV B | V B | VI B | VII B | VIII | I B | II B | III A | IV A | V A | VI A | VII A | O | ||
| 1 H | 2 He | ||||||||||||||||
| 3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne | ||||||||||
| 11 Na | 12 Mg | 13 Al | 14 Si | 15 P | 16 S | 17 Cl | 18 Ar | ||||||||||
| 19 K | 20 Ca | 21 Sc | 22 Ti | 23 V | 24 Cr | 25 Mn | 26 Fe | 27 Co | 28 Ni | 29 Cu | 30 Zn | 31 Ga | 32 Ge | 33 As | 34 Se | 35 Br | 36 Kr |
| 37 Rb | 38 Sr | 39 Y | 40 Zr | 41 Nb | 42 Mo | (43) | 44 Ru | 45 Rh | 46 Pd | 47 Ag | 48 Cd | 49 In | 50 Sn | 51 Sb | 52 Te | 53 I | 54 Xe |
| 55 Cs | 56 Ba | 57-71 Ln | 72 Hf | 73 Ta | 74 W | 75 Re | 76 Os | 77 Ir | 78 Pt | 79 Au | 80 Hg | 81 Tl | 82 Pb | 83 Bi | 84 Po | (85) | 86 Rn |
| (87) | 88 Ra | 89 Ac | 90 Th | 91 Pa | 92 U | (93) | (94) | (95) | (96) | (97) | (98) | (99) | |||||
| 57 La | 58 Ce | 59 Pr | 60 Nd | (61) | 62 Sm | 63 Eu | 64 Gd | 65 Tb | 66 Dy | 67 Ho | 68 Er | 69 Tm | 70 Yb | 71 Lu | |||
| Tableau périodique dans les années 1920-1930, suite aux travaux d'Henry Moseley. | |||||||||||||||||
Il était identique au tableau actuel, hormis pour ce qui avait trait à la septième période.
Concept des actinides de Glenn Seaborg
Le physicien américain Glenn Theodore Seaborg contribua dès 1942 au projet Manhattan dans l'équipe du physicien italien Enrico Fermi. Il était chargé d'isoler le plutonium — que lui-même avait synthétisé et caractérisé en février 1941 — de la matrice d'uranium au sein de laquelle il se formait. C'est au cours de ce travail qu'il développa une connaissance approfondie de la chimie particulière de ces éléments. Il établit ainsi que leur position dans le tableau périodique (l'uranium était alors placé sous le tungstène et le plutonium sous l'osmium) ne rendait pas compte de leurs propriétés.
En 1944, il parvint à synthétiser et à caractériser l'américium et le curium (éléments 95 et 96), ce qui lui permit de formaliser le concept des actinides, c'est-à-dire d'une nouvelle série chimique aux propriétés spécifiques et formée des éléments 89 à 103, située sous les lanthanides dans le tableau périodique, qui prit ainsi sa configuration actuelle. Seaborg conjectura également l'existence des superactinides, regroupant les éléments 121 à 153 et situés sous les actinides.
Le tableau périodique utilisé de nos jours est celui remanié en 1944 par Seaborg.