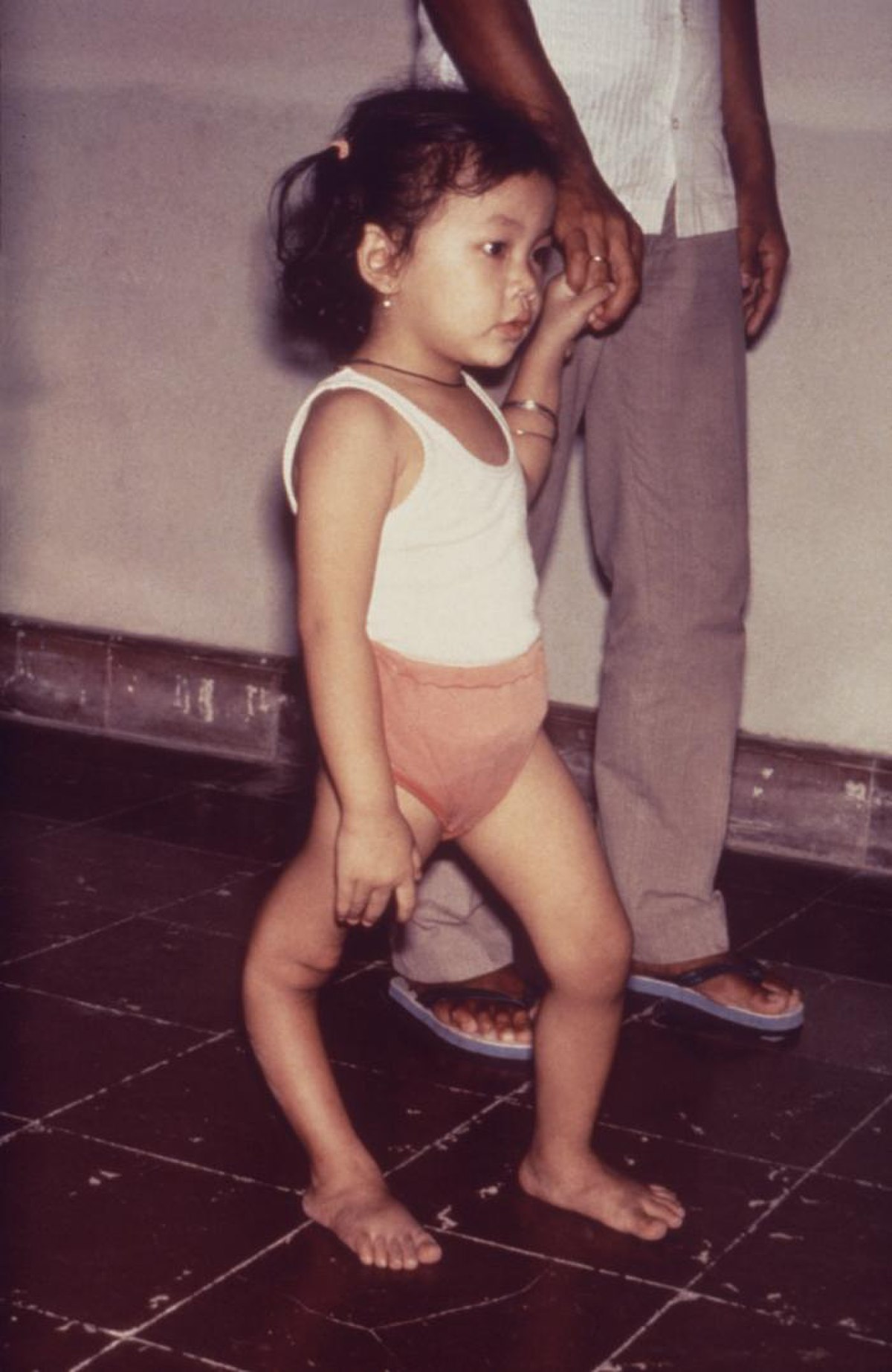Poliomyélite - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Poliomyélite (Maladie de Heine-Medin) Classification et ressources externes | ||
| CIM-10 | A80., B91. | |
|---|---|---|
| CIM-9 | 045, 138 | |
| DiseasesDB | 10209 | |
| MedlinePlus | 001402 | |
| eMedicine | ped/1843 pmr/6 | |
| MeSH | C02.182.600.700 | |
La poliomyélite (du grec polios (πολίός) « gris », -myelos (µυελός) « moelle » et -ite « inflammation »), également appelée maladie de Heine-Medin, paralysie spinale infantile ou simplement polio, est une maladie infectieuse aiguë et contagieuse spécifiquement humaine causée par trois virus à ARN du genre Entérovirus, les poliovirus.
L'infection à poliovirus, transmise par voie digestive (oro-fécale), est inapparente chez 90 à 95 % des sujets et se traduit dans le reste des cas par des symptômes le plus souvent bénins et non spécifiques (pharyngite, syndrome grippal, vomissements). L'infection du système nerveux central, la plus sérieuse, complique environ un cas sur cent. Elle entraîne une méningite et s'accompagne, dans la moitié des cas, d'une lésion des motoneurones de la corne antérieure de la moelle épinière qui définit la poliomyélite proprement dite ou poliomyélite antérieure aiguë. Il en résulte une paralysie flasque asymétrique intéressant le plus souvent les membres inférieurs.
La poliomyélite a été décrite et étudiée au XIXe siècle par Heine et Medin. Des années 1880 jusqu'à la seconde moitié du XXe siècle, la maladie a sévi dans le monde entier sur un mode épidémique et handicapé ou tué plusieurs millions de personnes. Les progrès de l'hygiène et surtout la vaccination, découverte par Salk et Sabin, ont permis un recul considérable de son incidence. Depuis 1988, l'éradication de la poliomyélite fait l'objet d'une initiative mondiale sous l'égide de l'OMS, de l'Unicef et du Rotary International. La campagne de vaccination de masse a fait passer son incidence de 350 000 nouveaux cas par an en 1988 à environ 1 500 en 2008 et son éradication est officielle sur tout le continent américain, en Europe et dans les régions OMS du Pacifique occidental, Chine comprise. En 2008, la maladie n'était encore endémique que dans quatre pays (Nigeria, Inde, Pakistan et Afghanistan) qui concentraient la quasi-totalité des cas. Une flambée de cas au Tadjikistan au début de l'année 2010 rappelle cependant que le virus circule toujours.
Historique
Bien que les premières épidémies de poliomyélite n'aient été identifiées qu'au XXe siècle, le poliovirus est probablement pathogène pour l'homme depuis plusieurs millénaires. Il est difficile cependant de dater les grandes épidémies d'avant le XXe siècle, l'obligation officielle de notifier les cas de polio, dans chaque pays, n'ayant été prise qu'au début du siècle (d'abord en Suède et en Norvège - 1905 -, puis aux USA en 1909, en Grande-Bretagne en 1911 et en France en 1936).
Jusqu'au XIXe siècle le poliovirus était un agent endémique et quiescent ; à partir de 1910, les épidémies deviennent régulières dans tout le monde industrialisé, principalement dans les villes et durant les mois d'été. Conjointement au progrès des savoirs, cette évolution de la maladie, avec ses crises épidémiques parfois dramatiques, conditionna la connaissance que les médecins – et la population – purent en avoir.
De l'antiquité à la découverte d'un virus
Certaines gravures de l'Égypte antique représentent des personnages handicapés moteurs avec certaines caractéristiques de la poliomyélite (adultes aux membres amyotrophiés, enfants marchant à l'aide de cannes) et des égyptologues anglais ont, il y a une cinquantaine d'années, reconnu des traces de polio sur un squelette datant de 3 400 ans avant J.-C.. Dans ce que la tradition impute à Hippocrate d'abord et à Gallien ensuite, on trouve quelques mentions de paralysies qui peuvent évoquer la poliomyélite.
Si les médecins Michael Underwood en 1784 puis Giovanni Battista Monteggia en 1813, sont crédités des premières descriptions de la poliomyélite : affection caractérisée par une période fébrile de quelques jours, suivie par une paralysie des jambes (symptômes parfois présentés par d'autres maladies comme la diphtérie), ce n'est qu'à partir des années 1860 que les médecins commencent à décrire les dommages spécifiques causés à la moelle épinière par la maladie, et cette dernière ne se voit baptisée de son nom scientifique de « poliomyélite » – qui signifie « inflammation de la substance grise de la moelle épinière » – qu’en 1874 (l'expression poliomyelitis anterior acuta est d'Adolphe Kussmaul). Jusqu'alors les symptômes de la poliomyélite avaient été décrits successivement, au début du XIXe siècle, sous les noms de paralysie dentaire, paralysie spinale infantile, paralysie essentielle de l'enfant ( Barthez et Rilliet, 1851), paralysie régressive, myélite des cornes antérieures (Séguin), téphromyélite (du grec tephros, « cendre grise » ; Charcot 1872), paralysie regressive (Barlow) et paralysie du matin(West, 1843).
C'est à Jakob Heine que l'on doit la première description précise, quoiqu'incomplète, de la maladie exposée dans son ouvrage de 1840 Beobachtungen über Lähmungszustände der untern Extremitäten und deren Behandlung. Il n'introduit toutefois le terme de Spinale Kinderlähmung que dans la seconde édition publiée en 1860 sous le titre Spinale Kinderlähmung. Monograph. Cet orthopédiste allemand crée l'entité clinique qu'il distingue clairement de la paralysie cérébrale infantile, et de l'hémiplégie. Il émet l'hypothèse du caractère épidémique de la maladie et suggère la localisation des lésions dans la corne antérieure de la moelle épinière.
Cette dernière hypothèse, également émise par Guillaume Duchenne de Boulogne dans De l'Électrisation fut confirmée par les autopsies pratiquées par André Victor Cornil en 1863 et par son élève Jean-Martin Charcot en 1870 qui y trouvèrent effectivement des altérations histologiques. Il semble qu'avant Duchenne, la localisation des lésions dans les cornes antérieures étaient bien acceptées concernant les paralysies spinales de l'enfant ; l'originalité de Duchenne aura été de suggérer semblable localisation pour la paralysie spinale de l'adulte.
En 1885 le neurologue allemand Adolf Strümpell décrit une maladie - portant depuis son nom - qu'il prend alors pour une forme cérébrale de la poliomyélite.
À l'automne 1881, un médecin suédois Nils August Bergenholtz diagnostique treize cas de poliomyélite antérieure aiguë (chez des enfants et deux adolescents) et en suggère le caractère épidémique. N'ayant pas été publiée, cette observation est restée inaperçue de ses contemporains (et des historiens jusqu'à récemment).
En 1887, un pédiatre suédois expérimenté Karl Oskar Medin qui n'avait jusqu'alors rencontré que des cas isolés de poliomyélite eut à faire face d'un coup à 44 cas à la polyclinique de Stockholm. Ses observations attentives lui permirent d'établir que la paralysie qui définissait jusqu'alors la maladie, n'était en fait que la deuxième phase d'un processus signalé d'abord par de la fièvre, des maux de tête et des malaises. Il établit aussi que la maladie pouvait se limiter à cette première phase. Enfin Medin fut aussi le premier à signaler le caractère épidémique de la maladie. Il publia ses travaux en 1890, année même où il acquit une reconnaissance internationale lors du 10e Congrès Médical International de Berlin.
Sur la base d'observations méthodiques faites pendant la vague épidémique de 1905 en Suède (qui fit 1 031 victimes), c'est le docteur Ivar Wickman qui devait apporter des preuves épidémiologiques de la contagiosité signalée précédemment par Oskar Medin. Enquêtant sur plus de mille cas, visitant lui-même les domiciles de plus de 300 patients, cherchant auprès des médecins des informations précises sur les autres, il arriva à la conclusion que la poliomyélite était souvent transmise par des personnes apparemment en bonne santé mais qui étaient tout de même affectées de façon mineure par la maladie, ce que Wickman lui-même appellera « poliomyélite abortive ». Sur ce point l'originalité de Wickman n'aura pas tant été de signaler ces cas bénins, que de souligner leur grande occurrence et leur rôle dans la propagation de la maladie. Par ailleurs, Wickman établit différents temps d'incubation de la maladie et en relève aussi la saisonnalité marquée. Il s'étonnera de ce que les malades n'étaient pas que des enfants : 21,4 % avaient plus de 14 ans. Enfin, c'est lui qui nomma la maladie maladie de Heine-Medin. Ses travaux conduisirent la Suède à rendre obligatoire la déclaration des cas de poliomyélite, tandis que l'épidémie de 1911-1913 donnant aux chercheurs l'occasion de confirmer ses travaux lui apportera une reconnaissance internationale.
La maîtrise des souches virales
La preuve définitive du caractère infectieux de la maladie est toutefois apportée par Karl Landsteiner et Erwin Popper en 1908'. Landsteiner injecta un extrait de la moelle épinière d'un jeune garçon décédé de polio à des rats, des cobayes, des souris ainsi qu'à deux singes (l'un Macaca mulatta, l'autre Papio hamadryas) : les singes - et seulement eux - furent rapidement paralysés, l'un des deux aux deux jambes ; à l'examen microscopique, leur moelle épinière présentait le même aspect que celle d'enfants décédés de polio.
Lors de ces expériences, Landsteiner et Popper ne réussirent toutefois pas à démontrer le caractère contagieux ; ils ne purent pas transmettre la maladie de singe à singe. Cela fut réalisé peu après en 1909 par plusieurs équipes : Römer, Flexner et Lewis, Leiner et von Wiesner, enfin Landsteiner et Levaditi (Landsteiner ayant rallié provisoirement l'Institut Pasteur pour profiter de son animalerie). La nature de l'agent infectieux ne put être établie. Flexner et Lewis n'ayant pu mettre en évidence aucun agent bactérien, concluent qu'il doit s'agir de ce qui était alors appelé un virus filtrant (la nature bactérienne de l'agent a eu ses défenseurs au moins jusqu'en 1952'').Malgré ces découvertes, la grande presse continuera encore à affirmer pendant des années aux États-Unis que le germe de la polio n'avait pas encore été découvert.
Sur la base d'expériences pratiquées sur des singes par eux-mêmes, mais aussi par Leiner et Von Wiesner, Simon Flexner et P.A. Lewis avancent en 1910 que le poliovirus accède au système nerveux central le long des voies nerveuses à partir de la muqueuse nasale. Une des raisons de cette conception erronée tient au fait que Flexner avait conduit ses expériences sur une des rares espèces de singes à ne pouvoir être infectée que par injections dans le système nerveux central. Par ailleurs - ainsi qu'on ne put le mettre en évidence qu'à la suite des découvertes d'Enders en 1949 - les expériences réitérées de Flexner conduisirent à une sélection des souches virales (MV strain ; mixed virus) qui ne purent plus se développer que sur des tissus d'origine nerveuse et n'induisant qu'une faible virémie. Cette conception d'un neurotropisme exclusif du poliovirus, ainsi que de son entrée par la voie nasale, dominante jusque dans les années 1930, occultera les résultats d'expériences qui ne rentraient pas dans son cadre explicatif.
C'est ce qui arriva aux travaux du Suédois Carl Kling (en collaboration avec Wilhelm Wernstedt et Alfred Pettersson) : prolongeant l'expérience de Lansteiner de 1909, il put montrer que l'injection d'extraits de tissus de la gorge, du larynx ou des intestins provenant d'adolescents décédés de polio produisait également une paralysie chez les singes. Il en conclut que la contamination pouvait se faire par un virus présent dans la salive ou les intestins des personnes atteintes : c'est ce que l'on a appelé la théorie de la voie intestinale ou également, en anglais, "the oral-fecal route". Par ailleurs, Kling put confirmer de manière expérimentale ce que Wickman avait conclut de ses observations, à savoir que des personnes ne présentant aucun symptôme pouvaient héberger le virus dans leur gorge ou leur intestin. Quand Kling et son équipe présentèrent leurs travaux à une conférence à Washington en 1912, Flexner, directeur du Rockfeller Institute for Medical Research – alors le pôle principal de recherche sur la polio – ne voulut leur accorder aucune crédibilité. Les chercheurs américains n'ayant pu aboutir aux résultats présentés par les Suédois après avoir repris leurs expériences, ils se détournèrent longtemps de la théorie de la voie intestinale. Il faudra attendre les travaux de Trask et de Paul de l'université Yale et surtout ceux d'Albert Sabin et de Robert Ward en 1941 pour que s'impose définitivement l'importance de la voie intestinale ; toutefois dès les années 1920 en Suède, les vues de Flexner s'accommodaient de celles de Kling fût-ce de façon marginale].
Les travaux de Kling ont sans doute souffert d'arriver aux États-Unis au moment où les chercheurs américains - dans le sillage de Milton Rosenau et bientôt sous la pression des évènements de 1916) - étaient enclins à voir dans la mouche des étables (Stomoxys calcitrans) le vecteur de la maladie.
Au même moment Simon Flexner découvrit des "germicidals substances" (appelées aujourd'hui anticorps), ayant d'abord extrait du sang de singes convalescents un sérum, puis en avoir injecté à d'autres singes en même temps que de la moelle infectée, il avait pu constater que ses sujets d'expérience ne manifestaient aucune paralysie. Arnold Netter avait fait une découverte semblable en 1909-1910 avec Constantin Levaditi. En 1915 il s'implique dans la promotion de ce sérum (issu de convalescents, humains ou simiens) qui fut largement utilisé lors de la sérieuse épidémie de 1916 aux États-Unis. Faute tant d'évaluations que de traitements alternatifs cette sérothérapie fut utilisée jusqu'en 1935 aux USA, jusqu'en 1940 au Canada.
Entre 1928 et 1931 Pierre Lépine démontre la survivance du virus de la poliomyélite dans les milieux extérieurs et, en particulier dans l'eau, la transmission du virus par la voie digestive au singe, l'action du chlore sur le virus. En 1929 dans le cadre de l’Office international d’hygiène publique, Carl Kling et Constantin Levaditi montrent sur la base d'études épidémiologiques menées en Saxe et en Roumanie, que la majorité des cas de polio ont lieu dans le voisinage de cours d'eaux : c'est l’hypothèse hydrique.
En 1931 comparant la souche Rockefeller MV avec une souche locale isolée à Melbourne, Sir Frank Macfarlane Burnet et Dame Jean MacNamara montrent qu'il existe au moins deux souches de virus (article publié en 1931 dans the British Journal of Experimental Pathology). Provenant de chercheurs inconnus situés sur un continent éloigné, ces résultats furent accueillis avec beaucoup de scepticisme. Leur importance ne fut vraiment reconnue que plus tard par Hammon, Francis et Rivers, à la lumière de l'échec des vaccins de 1935.
Dans les années 1934-35 apparurent deux vaccins américains rivaux et indépendants : l’un de type « inactivé » mis au point par le docteur Maurice Brodie, l’autre étant une version « atténuée » élaborée par le docteur John Kolmer. Malheureusement, leur utilisation à la hâte dans certaines parties des États-Unis se révéla inefficace, voire, dans certains cas, fatale. Pendant les vingt années qui suivirent cette expérience infructueuse, les chercheurs hésitèrent à se lancer dans un autre vaccin. C'est à cette période que le Docteur Claus W. Jungeblut proposa un traitement préventif et curatif par la vitamine C. Albert Sabin – déjà une autorité à l'époque – ne put obtenir les mêmes résultats ; le Docteur Fred R. Klenner proposera de nouveau cette approche en 1948 mais ne sera pas suivi. De la même façon, à la même époque, divers traitements par instillation nasale furent proposés et évalués, pour finir par être rejetés une fois leur inefficacité et leur nocivité établies.
En 1939 Charles Armstrong réussit à multiplier la souche Lansing dans le corps de souris, ce qui allait faciliter la recherche. Max Theiler, mais aussi Maurice Brodie semblent y être parvenus précédemment sans que cela ne soit relevé à l'époque.
En 1941 une équipe de l'Hôpital Johns Hopkins de Baltimore précisa le cycle du virus dans le corps humain. Ils montrèrent notamment que le virus devait pénétrer dans le sang avant de pouvoir accéder à la moelle épinière. Cette découverte ouvrait des perspectives pour un futur vaccin : si l'on arrivait à induire des anticorps dans le sang, alors le virus pourrait être neutralisé avant de provoquer des atteintes bulbaires.
En 1945 on pouvait encore s'interroger sur l'éventualité de réservoirs animaux du virus autres que les singes, par exemple les chiens'.
En 1946, Thomas Francis, dûment interrogé sur ce point, rappelle que les populations afro-américaines ne sont pas moins exposées à la poliomyélite ainsi que l'opinion commune semblait le croire'.
En 1949, au moment même où deux spécialistes éminents de la polio, Sir MacFarland Burnet et William Hammon, expriment leur pessimisme quant aux perspectives de contrôle de la maladie, trois Américains font une découverte majeure. Dans un article paru dans la revue Science du 28 janvier 1949, Enders, Weller et Robbins, font savoir qu'ils sont parvenus à cultiver le virus poliomyélitique - souche Lansing - sur des cellules embryonnaires humaines, sur des prépuces, des reins humains puis des reins de singes'. Cette découverte – dont l'importance ne fut pas immédiatement perçue par tous les chercheurs – allait rapidement donner un nouvel élan à la recherche. Dorénavant les chercheurs purent disposer de grandes quantités de virus à moindre frais : jusqu'alors, en dépit de la découverte d'Armstrong d'une part, et de la publication de Sabin et Olitsky de 1936 de l'autre, le virus n'était multiplié qu'in vivo, et sur des singes (Constantin Levaditi avait pourtant montré dès 1913 qu'il était possible de cultiver le virus sur des cellules d'origine non nerveuses). Dans l'éventualité de la mise au point d'un vaccin c'était aussi une garantie de sécurité. On connaissait en effet les risques de paralysie et de mort (0,4 % des inoculés) attachés au vaccin antirabique de Pasteur et qui résultaient d'une réaction immunitaire à l'injection de myéline contenue dans le vaccin : en cultivant le virus destiné au vaccin sur des cellules autres que d'origine nerveuse on pourrait s'affranchir de ce risque. Dans le cadre de ces travaux, Enders, Weller et Robbins découvrirent aussi un moyen rapide et peu cher de détection du virus (jusqu'alors la présence du virus n'était avérée que lorsqu'un singe avait été paralysé suite à une injection). Ces découvertes leur valurent le prix Nobel de médecine en 1954'. Peu de temps après, en 1952, les laboratoires Lederle firent savoir que deux de leurs équipes avaient réussi à cultiver un des virus de la poliomyélite (souche MEFI) sur des embryons de poulet.
En 1949 toujours, Bodian et Morgan établissent que quatorze souches différentes de poliovirus se ramènent à trois sérotypes (en 1951 un comité de la National Foundation for infantile Paralysis précisera que toutes les souches se regroupent bien en trois sérotypes, et seulement en trois).
En 1950, William Hammon (Université de Pittsburgh) parvint à purifier des gamma globulines à partir du plasma sanguin des patients ayant guéri de la poliomyélite. Hammon proposa l'injection de sérum anti-polio pour prévenir la maladie et réduire la sévérité des symptômes chez les patients atteints. Un grand essai clinique donna des résultats encourageants, laissant supposer que les gamma globulines anti-poliomyélitiques pouvaient prévenir la survenue d'une poliomyélite paralytique dans environ 80 % des cas. Cependant l'immunisation passive par sérothérapie s'avéra impossible à mettre en œuvre à grande échelle, principalement en raison de la quantité insuffisante de sérum disponible. La recherche se détourna de cette stratégie et se focalisa sur la mise au point du vaccin.
Dans le même temps, William Haast et Murray Sanders – financés par la March of Dimes – élaborèrent un traitement à base de venin de cobra, qui tomba dans l'oubli suite aux découvertes de Salk et Sabin.
L'ère des vaccins
En 1948, le Dr Isabel M. Morgan Mountain de la Johns Hopkins University démontra sur des singes l'efficacité d'un vaccin inactivé, ce qui eut une grande importance théorique : à l'époque le consensus scientifique voulait que, pour ce qui était de la poliomyélite, seul un vaccin vivant était capable de conférer une immunité. On doit rappeler ici que Jonas Salk fut à cette époque le collaborateur de Thomas Francis Jr. qui mit au point le premier vaccin contre la grippe – un vaccin vivant inactivé – en 1944.
Le 17 et 27 février 1950, Hilary Koprowski, assisté du Dr Jervis et de Mr Norton, inocule avec succès un vaccin vivant atténué (souche TN) à quelques enfants handicapés (après avoir obtenu une autorisation des parents,mais pas de ses autorités de tutelle)''. Koprowsky fait part de ses travaux à une réunion de la Foundation for infantile Paralysis en 1951 à Hershey.Cet essai vaccinal sur des êtres humains suscita un grand scandale aux États-Unis ; Koprowski s'aliéna ce faisant tout soutient des autorités gouvernementales qu'il dut alors chercher auprès du secteur privé .Sur le territoire américain, il poursuivit ses essais en 1952, en 1953, en 1954 et en 1955 .
En 1952 Dorothy Hortsmann de l'université Yale arriva enfin à mettre en évidence la présence du virus dans le sang (ce que confirmera David Bodian à Johns Hopkins Hospital).
Le 21 octobre 1952, le docteur Howard Howe de la Johns Hopkins University fait état d'un essai de vaccin trivalent à virus inactivé au formaldéhyde pratiqué sur six enfants handicapés (cinq autres enfants servant de contrôle). Les enfants ne furent pas soumis au virus : on mesura leur taux d'anticorps suite à l'inoculation des souches vaccinales'''.
Fin 1952, utilisant le milieu 199 de Hanks fourni par Connaught et après se l'être injecté à lui-même et à sa famille, Salk administra le vaccin aux résidents d’une institution pour enfants infirmes, le D.T. Watson Home for Crippled Children. Il conduisit un autre essai à la Polk State School en Pennsylvanie. À l'automne 1953, Salk avait testé son vaccin sur 637 personnes dans la région de Pittsburg. En 1953 Salk publie les résultats de ces essais, ce qui lui vaut immédiatement une renommée nationale' et des critiques : on craint que l'adjuvant utilisé – une huile minérale – ne soit cancérigène : il passe à une solution aqueuse.
La Fondation nationale pour la paralysie infantile demanda aux laboratoires de lui fournir la quantité de fluide viral nécessaire pour conduire un essai sur le terrain en double aveugle sans précédent aux États-Unis, qui devait commencer le 26 avril 1954. L’essai fut l’une des plus vastes expériences médicales de l’histoire. Il impliquait le suivi détaillé de près de 1 800 000 enfants de 5 à 8 ans qui, ayant reçu soit le Milieu 199 comme placebo soit le vrai vaccin, devaient être observés pour voir s’ils contractaient ou non la polio. Le 12 avril 1955, l'annonce du succès de l'expérience fut un énorme événement médiatique. Les fabricants américains lancèrent en hâte leur vaccin pour répondre à la demande. Cela se fit dans le cadre de la Poliomyelitis Vaccination Assistance Act.
Le 25 avril 1955, c'est le Cutter incident : on découvrit les premiers de 205 cas de polio dus au vaccin produit par les laboratoires Cutter, en Californie ; 79 étaient des enfants vaccinés, et les autres s’étaient trouvés en contact avec ces derniers. Les trois-quart des malades furent atteints de paralysie et onze périrent. Le 27 avril, le Médecin Général américain fit retirer tous les vaccins de Cutter du marché et le 8 mai, après le lancement d'une vaste enquête, tout le programme de vaccination aux États-Unis qui fut interrompu. Au total, cette première campagne de vaccination massive aura été marquée par la fourniture d'un important lot défectueux (virus vivant non atténué) aboutissant à près de 220 000 contaminations dont 70 000 malades, 164 paralysies sévères et dix décès.
En 1956 Sabin inocule son vaccin à 9 000 singes (macaques ?), 150 chimpanzés et 133 jeunes adultes dans une prison de l'Ohio. La même année, George Dick - connu pour avoir travaillé sur le vaccin atténué contre la fièvre jaune - invite H. Koprowski à conduire un vaste essai en Irlande. George Dick interrompra l'essai après avoir constaté que la souche vaccinale atténuée avait pu regagner de sa virulence.
En 1957, Salk et Pierre Lépine publient à quelques semaines d'intervalle les résultats de leurs travaux. Les deux vaccins diffèrent par les souches employées. Pour prévenir tout risque d'infection, Lépine a procédé à une double inactivation du virus, d'abord par le formol, puis par adjonction de béta-propiolactone.
En juillet 1957, l'OMS appelle à l'organisation d'essais à grande échelle pour les vaccins atténués qui respecteraient six critères de sécurité. C'est dans le prolongement de cette déclaration que le vaccin oral d'Albert Sabin fut testé à partir de 1957 sous l'égide de l'OMS en dehors des USA sur 80 millions de personnes (Russie, Hollande, Mexique, Chili, Suède et Japon). Le 18 août 1958, H. Koprowsky débute une vaste campagne de vaccination, avec le vaccin oral CHAT, au Congo belge, qui se prolongera jusqu'en 1960''.De 1958 à 1960, il vaccinera également 40,000 enfants en Allemagne et plus de sept millions en Pologne ( CHAT (sérotype 1)et/ou W-Fox(sérotype 3)) ; de 1960 à 1961 des essais ont lieu en Suisse ; et en 1961 en Croatie.Les essais conduits par Cox en Floride et à Berlin montrant que des souches vaccinales redevenaient virulentes, les laboratoires Lederle abandonnèrent les recherches avec les souches utilisées par Cox..
En 1959, le comité spécial crée un an auparavant par le National Institutes of Health afin d'évaluer les souches destinées au vaccin oral établit la supériorité de celles de Sabin sur celles de Koprowski et de Cox (et sur celles cultivées à l'université Yale). Cela conduira le Surgeon General à en recommander l'usage.
Le 24 avril 1960 c'est le Sabin Sunday : premier test massif du vaccin Sabin aux États-Unis. Le vaccin oral monovalent de type 1 (MOPV1) et celui de type 2 (MOPV2) obtinrent leur agrément en 1961 aux USA, le MOPV3 l'obtint en 1962.
En mai 1962 le Congrès américain examine un projet gouvernemental visant à édifier le cadre de futures campagnes de vaccinations massives (US Congressional Hearings HR10541). À l'occasion des multiples auditions menées à cet effet, le Congrès prend connaissance notamment de la position critique du Pr.Bernard Greenberg. Ce dernier signale l'existence de différents biais statistiques ayant conduit à surestimer l'effet des premières vaccinations antipolio – avec le vaccin Salk – qu'il juge responsables au contraire d'une augmentation des cas de polio. La loi est finalement adoptée la même année sous le nom de Vaccination Assistance Act PL 87-868 : elle débloque des fonds fédéraux pour l'achat de vaccins et pour l'établissement de statistiques.
En 1963 le vaccin oral Sabin trivalent (tOPV) obtient son autorisation.Suite à l'agrément du vaccin Sabin, le recours au vaccin Salk diminua rapidement pour ne représenter que 2% des vaccins polio utilisés annuellement aux USA.
La vaccination devient obligatoire et par conséquent gratuite en France en 1964. Elle avait précédemment été introduite dans le calendrier vaccinal français en 1958 (Salk), puis en 1962 (Sabin).
Une épidémie est enrayée aux États-Unis en 1965. Le taux de nouvelles contaminations est tombé à 1 pour 10 millions de personnes.
Fin 1987 le "vaccin Salk amélioré" ,"enhanced potency IPV" obtient son autorisation aux USA ( il avait été mis au point en 1978 ; procédé : culture sur cellules diploïdes humaines ; laboratoires Connaugh ).
En 1997 l'Advisory Committee on Immunization Practices recommande l'usage du vaccin inactivé pour les deux premières injections, les deux autres étant pratiquées avec un vaccin oral . Le 17 juin 1999 l'ACIP ne recommande plus que le seul vaccin inactivé.
Le 11 septembre 2000 la Royal Society de Londres invalide l'hypothèse de Edward Hooper postulant l'origine du sida dans les campagnes de vaccination antipolio menées par Koprowsky au Congo Belge à la fin des années 1950'.