Phosphore blanc - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Phosphore blanc | |||||
|---|---|---|---|---|---|
 | |||||
| Général | |||||
| No CAS | |||||
| No EINECS | |||||
| PubChem | |||||
| SMILES | |||||
| InChI | |||||
| Apparence | solide cristallin transparent blanc jaune d'apparence cireuse. Devient sombre lors d'exposition à la lumière. | ||||
| Propriétés chimiques | |||||
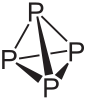
| Formule brute | P4 | ||||
| Masse molaire | 123,895048 ± 8,0E-6 g·mol-1 | ||||
| Propriétés physiques | |||||
| T° fusion | Se décompose au-dessous du point de fusion à 44 °C | ||||
| T° ébullition | 282 °C | ||||
| Solubilité | dans l'eau à 20 °C : 0,003 g·l-1 | ||||
| Masse volumique | 1,83 g·cm-3 | ||||
| T° d’auto-inflammation | 30 °C | ||||
| Point d’éclair | 30 °C | ||||
| Pression de vapeur saturante | 0,033 mbar à 20 °C, 0,076 mbar à 30 °C, 0,32 mbar à 50 °C | ||||
| Précautions | |||||
| | |||||
| |||||
| Phrases R : 17, 26/28, 35, 50, | |||||
| Phrases S : 1/2, 5, 26, 38, 45, 61, | |||||
| | |||||
| |||||
| | |||||
    Danger | |||||
| | |||||
Le phosphore blanc (aussi appelé phosphore jaune) est un allotrope commun de l'élément chimique phosphore qui permet des utilisations militaires extensives comme agent incendiaire, agent de protection par écran de fumée, et comme un composant d'arme anti-personnel capable de provoquer des brûlures graves. Couramment utilisé en tant que fumigène, il devient une arme chimique lorsqu'il est utilisé directement pour ses capacités offensives. Le protocole III additionnel à la Convention sur certaines armes classiques de l'ONU, signé en 1983, interdit son utilisation offensive, qui est considérée comme un crime de guerre.
Propriétés chimiques
Le phosphore blanc (aussi appelé phosphore jaune) est un solide blanc extrêmement inflammable et aux vapeurs corrosives.
Après combustion qui le transforme en pentoxyde de phosphore (P4O10), il absorbe l'humidité de l'air et des tissus vivants pour former de l'acide phosphorique (P4O10 + 6 H2O → 4 H3PO4) , il en résulte (lors de l'utilisation de bombes), une dissolution des tissus vivants (composés majoritairement d'eau), mais aucun dégâts aux vêtements.
C'est un explosif, mais ses capacités incendiaires (cœur de l'explosion) sont nettement supérieures au napalm, le phosphore qui ne brule pas s'échappe sous la forme d'un nuage corrosif, ce qui le classe dans la catégorie des armes chimiques. Lors d'utilisations offensives, les concentrations de phosphore sont si élevées que le nuage blanc en question est souvent beaucoup plus meurtrier que l'explosion.
La manipulation de bombes au phosphore nécessite de grandes précautions. Les transports se font dans un lieu frais, sous l'eau et dans des caisses, par exemple.
En 1983 l'Onu interdit son utilisation offensive et classe son utilisation de crime de guerre.



