N-Butyllithium - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| n-Butyllithium | ||||
|---|---|---|---|---|
| ||||
| Général | ||||
| Nom IUPAC | ||||
| Synonymes | Buli | |||
| No CAS | ||||
| No EINECS | ||||
| PubChem | ||||
| ChEBI | ||||
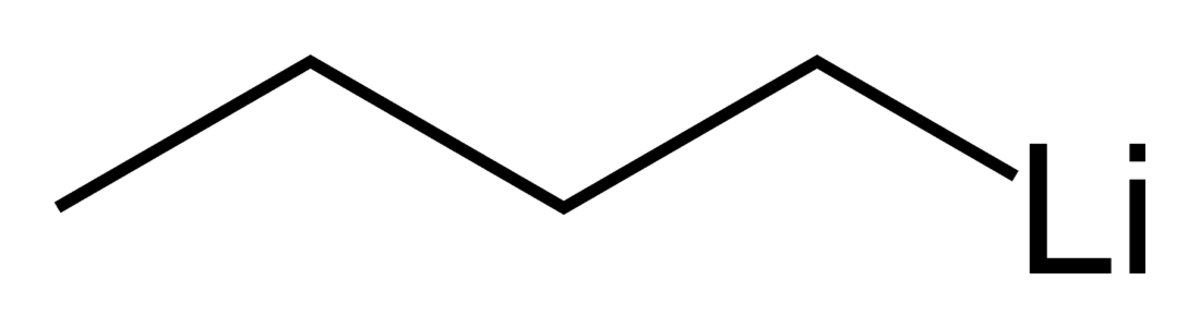
| SMILES | ||||
| InChI | ||||
| Apparence | solide cristallin incolore, instable et obtenu habituellement en solution légèrement jaune | |||
| Propriétés chimiques | ||||
| Formule brute | C4H9Li | |||
| Masse molaire | 64,055 ± 0,006 g·mol-1 | |||
| Propriétés physiques | ||||
| T° fusion | -76 °C | |||
| T° ébullition | 69 °C | |||
| Masse volumique | 0,68 g·cm-3 à 20 °C | |||
| Point d’éclair | -22 °C | |||
| Pression de vapeur saturante | 163 mbar à 20 °C | |||
| Précautions | ||||
| | ||||
| ||||
| Phrases R : 11, 14/15, 17, 34, 48/20, 51/53, 62, 65, 67, | ||||
| Phrases S : 7/8, 16, 26, 36/37/39, 45, 61, | ||||
| | ||||
| ||||
| | ||||

| ||||
| | ||||
Le n-butyllithium (en abrégé n-BuLi) est le plus important des réactifs organolithiens. Il est d'un très large emploi comme initiateur de polymérisation dans la production d'élastomères comme le polybutadiène ou le styrène-butadiène (SBS) et comme une base forte (superbase) en synthèse organique aussi bien à une échelle industrielle que dans les laboratoires.
Le n-butyllithium est commercialement disponible en solution (15%, 25%, 2 M, 2.5 M, 10 M, etc.) dans des alcanes comme le pentane, les hexanes et les heptanes, ou dans des éthers comme le diéthyl éther et le THF. La production mondiale annuelle et la consommation de butyllithium et des autres composés organolithiens sont estimées à 1 800 tonnes.
Malgré le fait qu'il soit un solide incolore, la n-butyllithium est usuellement trouvé comme une solution jaune pâle (alcane). De telles solutions sont stables indéfiniment si elles sont correctement stockées mais en pratique, elles se dégradent avec l'âge. Un fin précipité blanc (hydroxyde de lithium) se dépose et la couleur vire à l'orange.
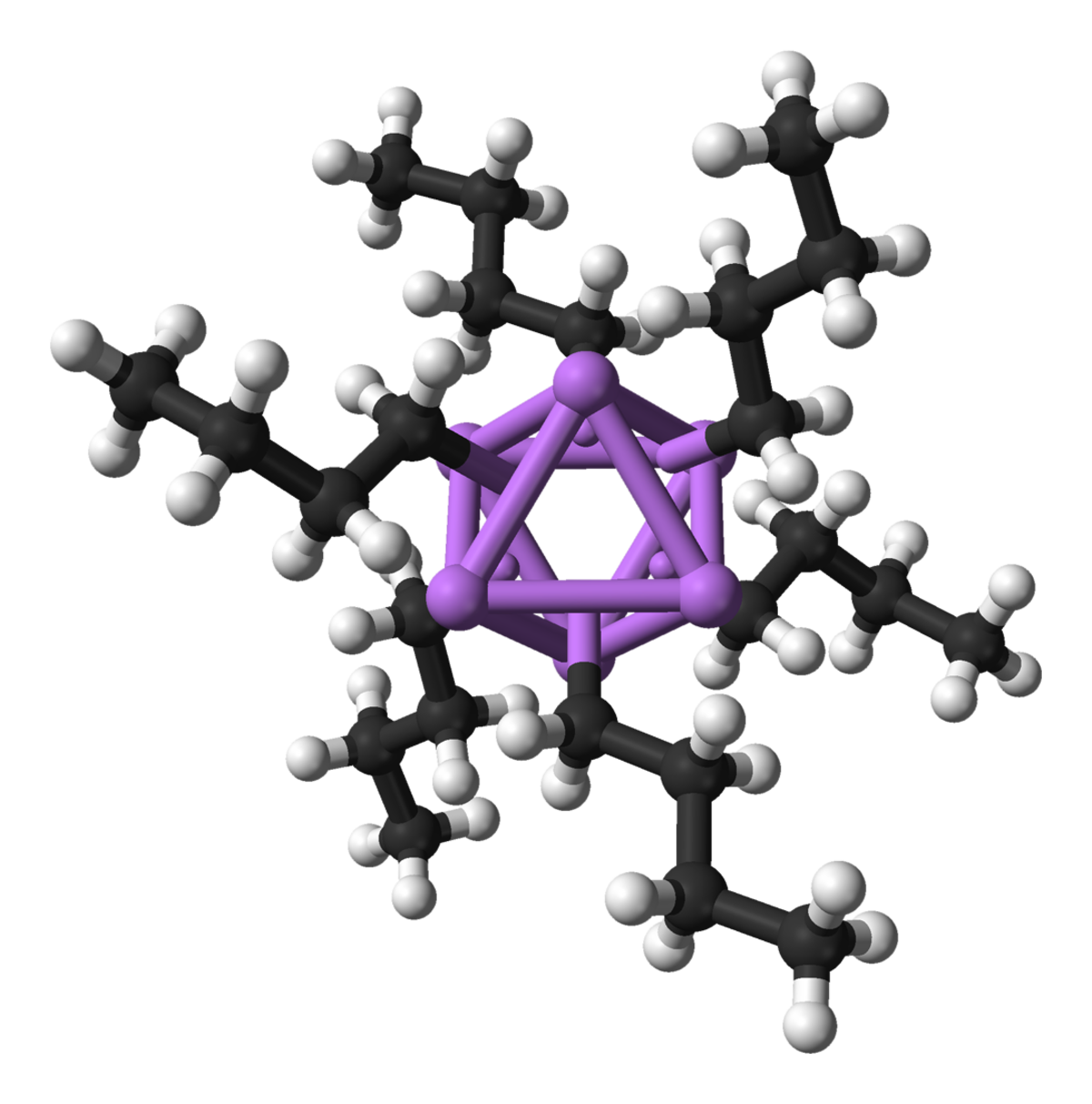
Structure et liaison
Le n-BuLi est sous forme de cluster à l'état solide et en solution dans la plupart des solvants. Cette tendance à s'agréger est commune aux composés organolithiens. Ces agrégats sont maintenus compacts par les liaisons covalentes délocalisées entre le lithium et le carbone terminal des chaînes butyle. Dans le cas du n-BuLi, les clusters sont tétramériques (dans le diéthyl éther) ou hexamériques (dans l'hexane). Les clusters tétramériques ont une structure de cubane distordu avec les lithiums et des groupes CH2 alternativement disposés sur les sommets. Une description équivalente est de voir le tétramère comme un tétraèdre Li4 interpénétré par un autre tétraèdre [CH2]4. Les liaisons à l'intérieur du cluster sont du même type que celles utilisées pour décrire le diborane, mais sont plus complexes puisqu'elles impliquent huit atomes. Reflétant son caractère déficitaire en électron, le n-butyllithium est très réactif vis-à-vis des bases de Lewis.
Du fait de la grande différence d'électronégativité entre le carbone (2,55) et le lithium (0,98), la liaison Li-C est fortement polarisée. La séparation des charges a été estimée vers 55-95%. Ainsi, même si pour des raisons pratiques, n-BuLi est souvent considéré comme un réactif qui agit via l'anion butyl, n-Bu−, avec le cation Li+, ce modèle est incorrect, n-BuLi n'est pas ionique.





















































