Molécule d'eau - Définition
La liste des auteurs de cet article est disponible ici.
Production de l'eau pure
L’eau pure est un excellent solvant et absorbe facilement les gaz qui entrent à son contact. Par conséquent, l’eau pure est pratiquement introuvable. Les laboratoires d’analyses ont néanmoins besoin de cette eau pure pour réaliser des analyses fiables. Ils vont donc faire appel, au cours du temps, à des techniques de purification de plus en plus sophistiquées.
Après l’eau distillée, bidistillée, déminéralisée, déionisée, la technique progresse vers une eau de plus en plus pure, donc coûteuse à produire et de plus en plus instable.
Chimie
Nature dipolaire
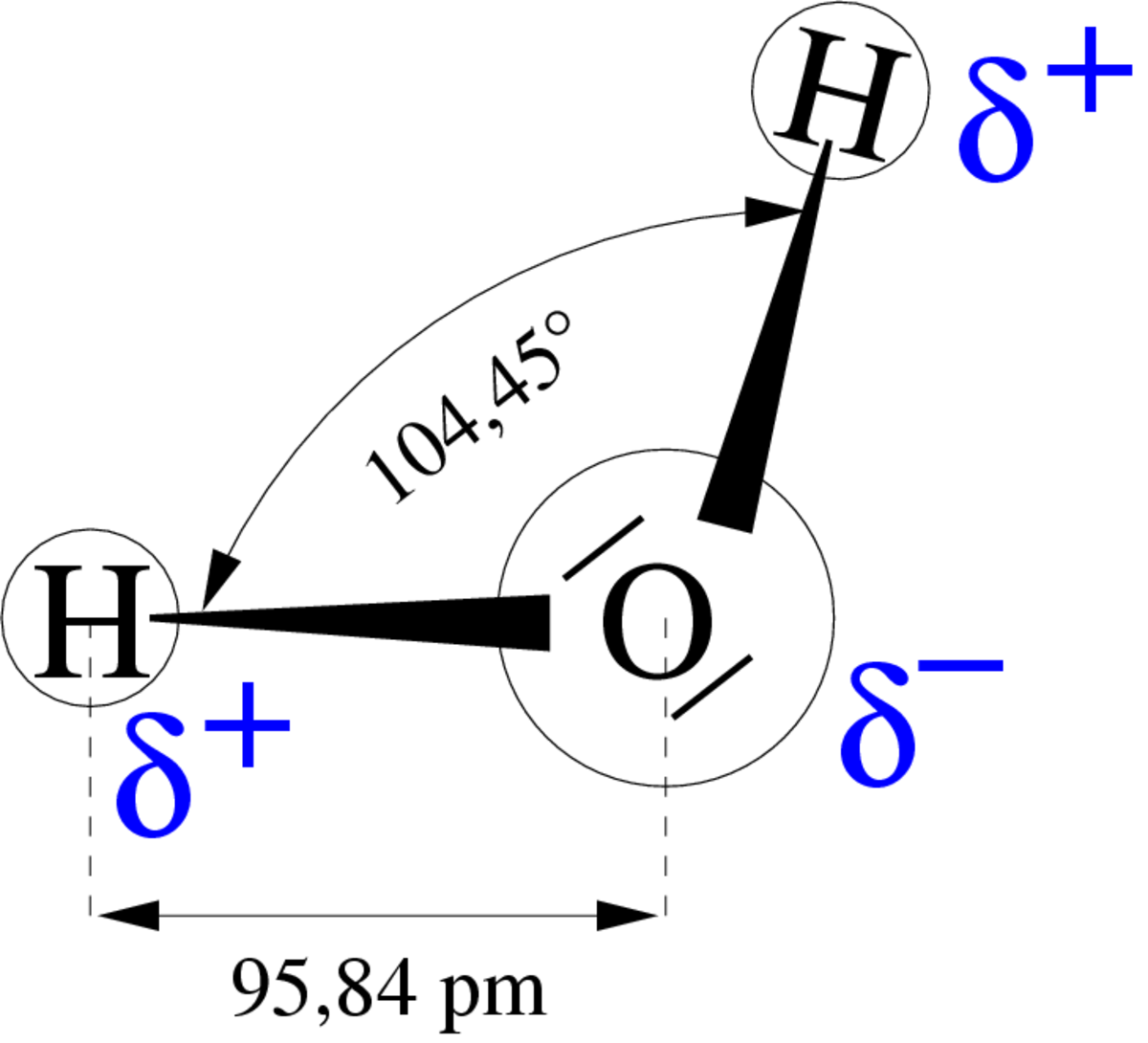
Une propriété très importante de l’eau est sa nature polaire. La molécule d’eau forme un angle de 104,45 ° au niveau de l’atome d’oxygène entre les deux liaisons avec les atomes d’hydrogène. Puisque l’oxygène a une électronégativité plus forte que l’hydrogène, l’atome d’oxygène a une charge partielle négative δ-, alors que les atomes d’hydrogène ont une charge partielle positive δ+. Une molécule avec une telle différence de charge est appelée un dipôle (molécule polaire). Ainsi, l’eau a un moment dipolaire de 1,83 Debye. Cette polarité fait que les molécules d’eau s’attirent les unes les autres, le côté positif de l’une attirant le côté négatif d’une autre. Un tel lien électrique entre deux molécules s’appelle une liaison hydrogène.
Cette polarisation permet aussi à la molécule d’eau de dissoudre les corps ioniques, en particulier les sels, en entourant chaque ion d’une coque de molécules d’eau par un phénomène de solvatation.
Cette force d’attraction, relativement faible par rapport aux liaisons chimiques covalentes de la molécule elle-même, explique certaines propriétés comme le point d’ébullition élevé (quantité d’énergie calorifique nécessaire pour briser les liaisons hydrogène), ainsi qu’une capacité calorifique élevée.
À cause des liaisons hydrogènes également, la densité de l’eau liquide est supérieure à la densité de la glace.
Autoprotolyse
L’eau se dissocie naturellement en ion oxonium H3O+ (aussi appelé hydronium) et ion hydroxyde OH− :
- 2 H2O = H3O+ + OH−
La réaction est dite d’autodissociation ou d’autoprotolyse.
Dans cette réaction, l’eau joue à la fois le rôle d’acide et de base : comme acide, elle perd un proton H+ et devient l’ion hydroxyde OH− ; comme base elle gagne un proton H+ et devient l’ion oxonium HO+. On dit donc que c’est une espèce amphotère ou un ampholyte.
La constante d’équilibre de cette réaction est très faible (10-14 à 25 °C) ; le nombre d’ions oxonium et hydroxyde formés est donc très minoritaire devant le nombre de molécules d’eau.
Du fait de l’équilibre, à une température donnée, le produit des concentrations de ces ions est constant, égal à la constante de dissociation. À 25 °C, il vaut :
- [HO+].[OH−] = 10−14
Dans l’eau pure, les ions H3O+ et OH− sont issus uniquement de l’autoprotolyse de l’eau, ils sont donc présents en concentrations égales, donc :
- [H3O+] = [OH−] = 1×10−7 mol·l−1 (à 25 °C)
Le pH étant défini à partir de la concentration en ions oxonium (pH = −log [H3O+]), à 25 °C, le pH de l’eau pure vaut donc 7, il est dit neutre.
Cet équilibre acide/base est d’une importance capitale en chimie minérale comme en chimie organique.
Comme solvant

Grâce à sa polarité, l’eau est un excellent solvant. Quand un composé ionique ou polaire pénètre dans l’eau, il est entouré de molécules d’eau. La relative petite taille de ces molécules d’eau fait que plusieurs d’entre elles entourent la molécule de soluté. Les dipôles négatifs de l’eau attirent les régions positivement chargées du soluté, et vice versa pour les dipôles positifs. L’eau fait un excellent écran aux interactions électriques (la permittivité électrique ε de l’eau est de 78,5 à 25 °C), il dissocie donc facilement les ions.
En général, les substances ioniques et polaires comme les acides, alcools, et sels se dissolvent facilement dans l’eau, et les substances non-polaires comme les huiles et les graisses se dissolvent difficilement. Ces substances non-polaires restent ensemble dans l’eau car il est énergétiquement plus facile pour les molécules d’eau de former des liaison hydrogène entre elles que de s’engager dans des interactions de van der Waals avec les molécules non polaires.
Un exemple de soluté ionique est le sel de cuisine alias chlorure de sodium, NaCl, qui se sépare en cations Na+ et anions Cl−, chacun entouré de molécules d’eau. Les ions sont alors facilement transportés loin de leur matrice cristalline. Un exemple de soluté non ionique est le sucre de table. Les dipôles des molécules d’eau forment des liaisons hydrogène avec les régions dipolaire de la molécule de sucre.
Cette faculté de solvant de l’eau est vitale en biologie, parce que certaines réactions biochimiques n’ont lieu qu’en solution (par exemple, réactions dans le cytoplasme ou le sang.)
C’est pourquoi, pour le moment, l’eau liquide est considérée comme indispensable à la vie et est activement recherchée sur les divers astres du système solaire, notamment sur Mars et Europe, une lune de Jupiter.
Tension superficielle
Les liaisons hydrogène confèrent à l’eau une grande tension superficielle et une grande cohésion. Cela se voit quand de petites quantités d’eau sont posées sur une surface non soluble et que l’eau reste ensemble sous forme de gouttes. Cette propriété qui se manifeste par la capillarité est utile dans le transport vertical de l’eau chez les végétaux et nuisible avec la remontée d’humidité dans les murs de maisons.
Conductivité
L’eau pure est un mauvais conducteur d’électricité. Mais puisque l’eau est un bon solvant, elle contient souvent une grande quantité de solutés dissouts, le plus souvent des ions. Si l’eau contient de telles impuretés, elle peut conduire l’électricité plus facilement. Le stator des très gros alternateurs est refroidi par circulation d’eau déionisée dans les conducteurs creux de l’enroulement. Malgré les différences de potentiel de plusieurs dizaines de milliers de volts entre le circuit de refroidissement et les conducteurs électriques, il n’y a pas de problèmes de fuite de courant. Voir conductivité électrique (mesure).
La pureté de l’eau peut être mesurée par sa résistance à un courant électrique.
Décomposition (thermolyse et électrolyse)
La première décomposition de l’eau fut faite par Lavoisier, en faisant passer de la vapeur d’eau sur du fer chauffé au rouge (thermolyse). Ce faisant, il établit que l’eau n’était pas un élément mais un corps chimique composé de plusieurs éléments.
La thermolyse de l’eau commence à devenir significative vers 750 °C et elle est totale vers 3 000 °C. La réaction produit du dioxygène et du dihydrogène :
- 2 H2O → 2 H + O
L’autre manière de décomposer l’eau est l’électrolyse. Sous l’effet d’une tension appliquée entre deux électrodes plongées dans de l’eau, l’eau peut être décomposée en dihydrogène et dioxygène. Les molécules d’eau se dissocient naturellement en ions HO+ et OH−, qui sont attirés par la cathode et l’anode respectivement mais comme cette dissociation est faible dans la pratique on a recours à des catalyseurs comme l’acide sulfurique ou l’hydroxyde de sodium. À l’anode, quatre ions OH− se combinent pour former des molécules de dioxygène O, deux molécules d’eau, et libérer quatre électrons. Les molécules de dioxygène ainsi produites s’échappent sous forme de bulles de gaz vers la surface, où elles peuvent être collectées. Dans le même temps, à la cathode, il y a une libération de deux molécules de dihydrogène H avec utilisation de quatre électrons.
- 4OH− → O + 2H2O + 4e−
- 4H3O+ + 4e− → 2H + 4H2O