Faibles doses d'irradiation - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
En radiobiologie, les faibles doses d'irradiation sont des accumulations de petites irradiations d'origine variées, qui se situent à un niveau très faible, largement inférieur à celui où l'on commence à voir apparaître un effet déterministe (brûlures ou syndrome d'irradiation aiguë pour des expositions supérieures au gray) ou un effet stochastique (leucémies ou autres formes de cancers, ou mutation génétique pour des expositions supérieures au centigray).
Si ces faibles doses ont un effet, celui-ci ne peut pas être étudié statistiquement, par des études épidémiologiques directes. L’estimation des risques pour des faibles doses d’irradiation est basée sur l’extrapolation des effets cancérogènes observés à fortes doses, entre 0,2 et 3 sieverts (1 Sv = 1 Gy corrigé pour les effets de dose équivalente et de dose efficace).
À un niveau microscopique, il est certain que l'effet physique et chimique élémentaire d'un rayonnement ne dépend que de sa nature, et non de la dose. Cependant, la traduction biologique de cet effet jusqu'à sa manifestation macroscopique est un processus complexe, que l'on commence à peine à découvrir. Globalement, l'effet exact de ces faibles doses d'irradiations, ainsi que la relation dose-effet associée, sont encore des questions ouvertes.
C'est principalement dans ce domaine de doses, inférieures à une dizaine de millisieverts par an, que la plus grande partie de la population se trouve exposée, que ce soit par l'irradiation naturelle (principalement due au radon), ou par des examens radiologiques, voire par les activités de l'industrie nucléaire. Ceci en fait un sujet polémique, et qui a une incidence directe sur l'optimisation des politiques de radioprotection et de santé publique.
Approche linéaire historique
Études des fortes doses
L'effet nocif des irradiations aux fortes doses a été identifié dès le début du XXe siècle : Henri Becquerel et Pierre et Marie Curie ont présenté des brûlures parce qu'ils manipulaient sans précaution des produits radioactifs. La première étude documentant les effets sur la peau date de 1896. Le premier cancer de la peau radio-induit est décrit en 1902, le premier cancer expérimental en 1910. La guerre de 1914-1918 a vu un développement massif de la radiologie médicale, et le nombre de lésions radio-induites a été très élevé. L’action mutagène possible est mise en évidence en 1927.
De nombreuses études épidémiologiques ont permis d'estimer les risques des rayonnements ionisants pour des expositions entre 0,2 et 5 sievert. Il n'y a guère de contestation sur le fait que ces doses produisent des effets observables, et ces effets sont parfois compatibles avec une loi linéaire (il faut rappeler que la théorie linéaire sans seuil est contredite par l’observation des cancers osseux induits par le radium 226 et des cancers du foie induits par le Thorotrast, qu’elle n’est pas compatible avec les leucémies induites à Hiroshima et chez les patients traités par l’iode radioactif).
Pour les effets stochastiques, la relation entre dose d'irradiation et effet (principalement, l'apparition de cancers à long terme) se fonde principalement sur la cohorte des survivants des bombardements atomiques de Hiroshima et Nagasaki. En moyenne, l'observation de ces cohortes de survivants après un demi-siècle a montré (sur une cohorte de près de 90 000 survivants) un excès de décès de 334 cancers et 231 leucémies. Cet effet est significatif pour les doses supérieures à 0,1 sievert, et le nombre de cancers augmente avec la dose reçue d'une manière grossièrement proportionnelle.
Si l'on divise l'excès de cancers par l'exposition moyenne, on constate que pour ces expositions, l'excès de cancers est de l'ordre de 5% de cancer par sievert. Il y a cependant de fortes incertitudes sur les doses effectivement reçues par les différents survivants, et ceux exposés à de très fortes doses ont majoritairement succombé aux conséquences immédiates des explosions. C'est là le fondement de l'estimation du risque retenue par la CIPR, de l'ordre de 5% de cancer par sievert.
Mais ces études ne permettent d'observer directement que l'effet de doses relativement fortes (> 100 mSv). Est-il légitime d'extrapoler ces conclusions aux domaines des faibles doses, pour lesquelles on n'observe pas d'effet direct ? Cette question est polémique.
Limites des études statistiques
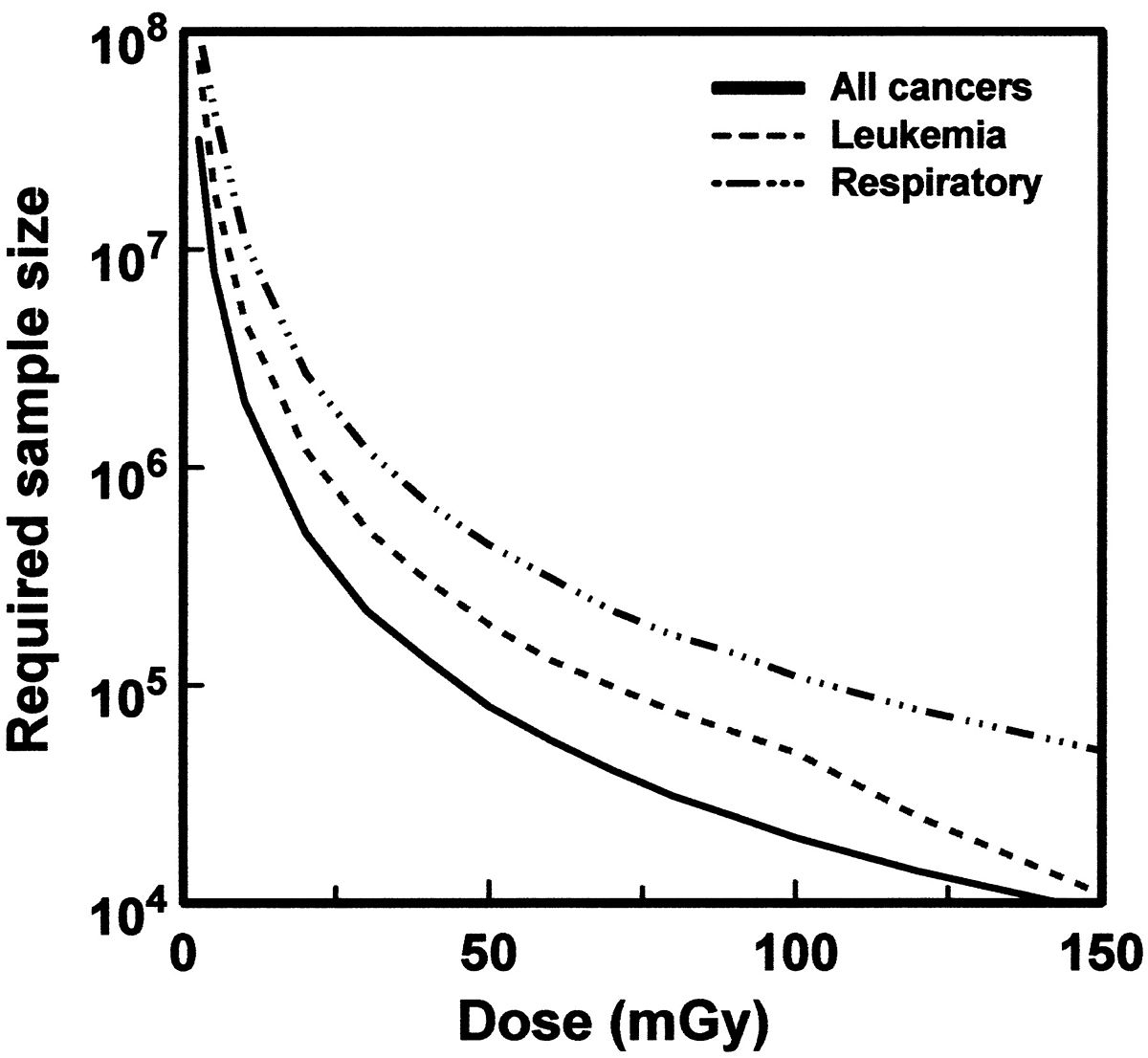
Il n'est pas possible d'observer directement un faible effet de faibles doses d'irradiation, parce que par ailleurs des cancers apparaissent dans la population de manière aléatoire, avec une certaine moyenne, et des variations aléatoires autour de cette moyenne qui provoquent un « bruit » statistique. Pour que l'effet d'une faible dose soit observable, il doit être nettement supérieur au niveau des variations aléatoires (le rapport signal sur bruit doit être suffisant). Comme le signal augmente proportionnellement à la taille N de la population, et le bruit des fluctuations, proportionnel à l'écart-type, varie avec la racine carrée de N, le rapport signal/bruit s'améliore comme la racine de N. Pour observer un effet avec une précision de l'ordre du pour-cent, il faut une population N de l'ordre de 10 000 ; pour observer l'effet supposé des faibles doses, qui est mille fois plus faible, il faudra une population N un million de fois plus importante - c'est-à-dire faire un suivi personnel de toute la population terrestre, ce qui est évidemment impossible. S'il faut un échantillon de 500 personnes pour quantifier l'effet d'une dose de 1000 mSv, il faudra (dans l'hypothèse où l'effet est linéaire) un échantillon de 50 000 personnes pour quantifier l'effet d'une dose de 100 mSv, et ≈5 millions pour 10 mSv.
Sur le plan épidémiologique, il n’y a pas de divergence, tous les rapports considèrent qu’il n’y a pas de preuve d’un effet cancérogène pour des doses inférieures à 100 mSv. Les études épidémiologiques disponibles ne décèlent aucun effet pour des doses inférieures à 100 mSv, soit qu’il n’en existe pas, soit que la puissance statistique des enquêtes ait été insuffisante pour les détecter.
Cependant, bien qu’à de faibles niveaux de dose d’irradiation, aucun effet sur la santé n’ait été observé au cours de la très grande majorité des études épidémiologiques, l’absence d’effets décelables ne permet pas d’exclure l’existence d’un risque.
L'approche « linéaire sans seuil »
L'approche la plus simple est celle du modèle « linéaire sans seuil », qui postule que le nombre de cancers induits par une exposition aux rayonnements ionisants varie de manière linéaire avec la dose reçue, et sans seuil en deçà duquel on puisse considérer qu'une exposition serait sans effet.
Le modèle linéaire découle directement de l'image de la cible : a priori, on peut considérer que chaque rayonnement ionisant a une certaine probabilité de toucher sa « cible » d'ADN, chaque impact provoque une anomalie génétique qui dérègle la cellule et a une certaine probabilité de déclencher un cancer ; à partir du moment où une seule particule est susceptible de provoquer un cancer (avec une probabilité si faible soit-elle), la probabilité globale d'observer un cancer ne peut que croître linéairement avec la dose reçue.
La justification avancée par certains auteurs se fonde sur les arguments suivants :
- L'étude statistique directe montre qu'une augmentation du risque de cancer peut être statistiquement mise en évidence pour des expositions aux rayons X pour des doses (par organe) de 10 mGy. L’effet cancérogène de doses de l’ordre de 10 mSv est prouvé chez l’homme par les résultats des études sur l’irradiation in utero. À partir de 10 mGy, la relation linéaire sans seuil rend compte de manière correcte de la relation dose-effet pour l’induction de tumeurs solides dans la cohorte d’Hiroshima et Nagasaki.
- Aux doses inférieures à 10 mSv, les cellules irradiées ne sont traversées que par une seule trajectoire (ou un très faible nombre de trajectoires indépendantes), et il n’y a pas d’interaction entre les différents événements physiques initiés le long des différentes trajectoires : en l'absence d'interaction, l'effet de chaque trajectoire sur une cellule est un évènement stochastique indépendant.
- La nature des lésions ainsi causées et la probabilité de réparation fidèle ou fautive et d’élimination par la mort des cellules lésées ne dépendent ni de la dose ni du débit. Réduire la dose ne fait que diminuer le nombre de cellules touchées, mais en l'absence d'interaction, le dommage initial et le devenir d'une cellule touchée sont les mêmes, que la dose macroscopique soit 10 mGy ou plus petite. Rien ne permet de penser que des processus biologiques soient par exemple actifs à 10 mGy et inactivés à 1 mGy, ou vice versa.
- Le cancer est la conséquence directe et aléatoire d’une lésion de l’ADN dans une cellule apte à se diviser et la probabilité pour qu’une cellule initiée donne naissance à un cancer n’est pas influencée par les lésions dans les cellules voisines et les tissus.