Cyanure - Définition
La liste des auteurs de cet article est disponible ici.
Introduction
| Cyanure | |
|---|---|
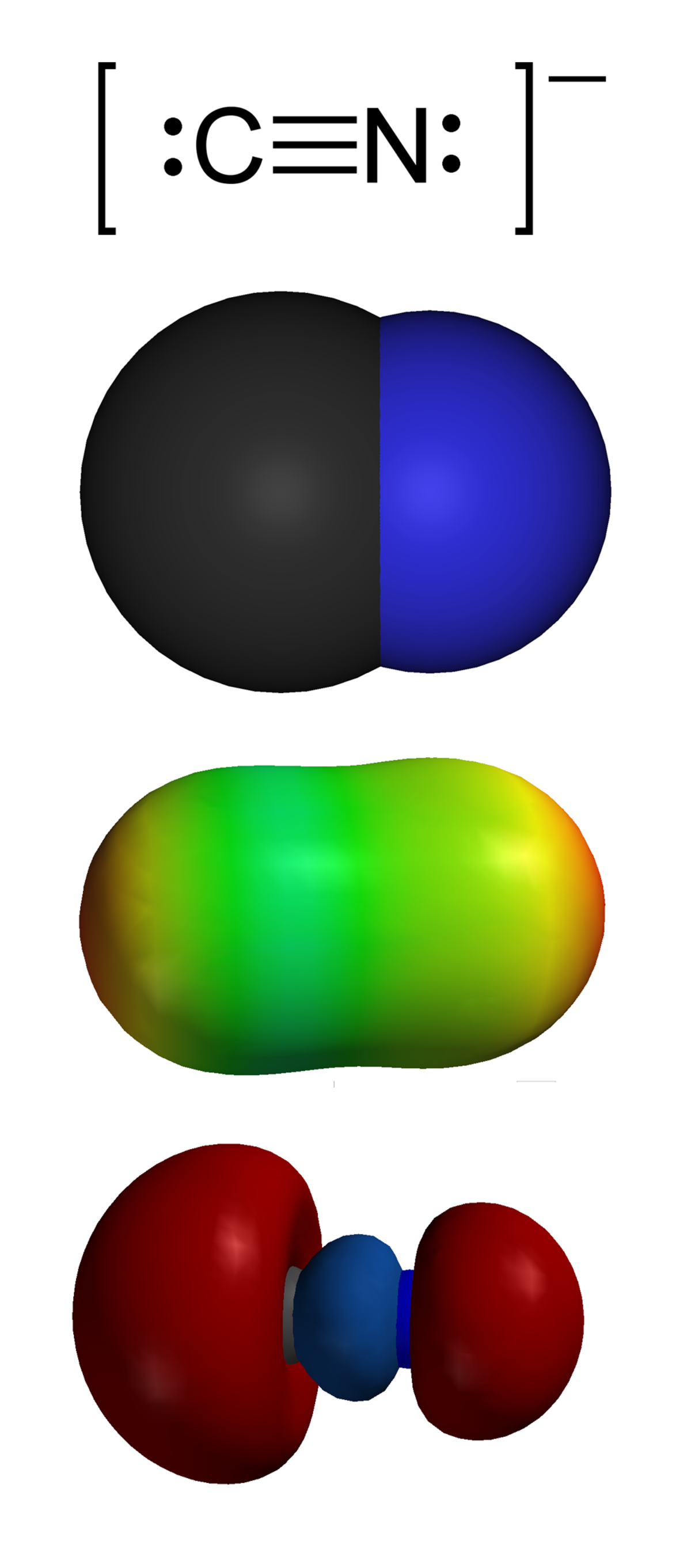
| |
| Général | |
| No CAS | |
| Propriétés chimiques | |
| Formule brute | CN- |
| Masse molaire | 26,0174 ± 0,001 g·mol-1 |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 13,5984 eV (gaz) |
| | |
Les cyanures sont les composés de l'anion CN-, formé d'un atome de carbone lié par une liaison triple à un atome d'azote. L'ion CN- est la base conjuguée de l'acide cyanhydrique.
- Structure (ou formule) de Lewis : -|C≡N|
- Réaction acido-basique : H-C≡N = N≡C- + H+
Formes
Les sels de cet ion sont extrêmement toxiques, de même que l'acide qui leur est associé : l'acide cyanhydrique. Dans le langage courant, on utilise souvent le terme cyanure pour désigner le cyanure de potassium (KCN).
Les ferrocyanures (ou hexacyanoferrates II) Fe(CN)64 -, en revanche, sont pratiquement inoffensifs. Les ferrocyanures de calcium, de sodium et de potassium sont des additifs alimentaires (anti-agglomérants) respectivement référencés E 538, E 535 et E 536.
Le ferrocyanure de potassium est autorisé pour le collage des vins blancs ou rosés présentant des excès de fer en vue d'une mise en bouteilles en raison de sa capacité à faire précipiter les métaux (fer et cuivre notamment) responsables de casses. Ce traitement est à l'origine de la création du diplôme national d'œnologie en 1955 car les pouvoirs publics ont alors estimé qu'il était nécessaire de former des techniciens compétents et responsables pour réaliser l'opération. Le déferrage des vins rouges par collage au ferrocyanure de potassium est interdit car il est impossible de contrôler l'absence de résidus de fer (dissous ou en suspension) dans le vin du fait de la coloration du vin liée à la présence d'anthocyanes.
Historiquement, le collage au ferrocyanure de potassium des vins présentant des sucres résiduels était pratiqué et permettait de réduire la teneur du vin en micronutrients utilisables par les levures responsables de refermentations spontanées.
Les ferricyanures (ou hexacyanoferrates III) Fe(CN)63- présentent également une faible toxicité.
Sécurité
Toxicité
Le cyanure se fixe sur les atomes de fer contenus dans l'hémoglobine et la cytochrome oxydase. Cette dernière est responsable du transport et de l'utilisation de l'oxygène dans la chaîne respiratoire mitochondriale. Il est à signaler que, si la fixation de cyanure sur l'hémoglobine déplace la courbe de saturation de l'hémoglobine vers la gauche et diminue de ce fait l'extraction d'oxygène par les tissus, ce mécanisme est modeste dans la mort par intoxication au cyanure.
Il est particulièrement redoutable sous forme de cyanure d'hydrogène, composé volatile et très toxique. Ce gaz se forme notamment lorsque les cyanures sont acidifiés (en solution ou par les sucs gastriques après ingestion). Il est utilisable pour ses propriétés anoxiantes comme arme chimique.
L'intoxication au cyanure peut se produire simplement lors de l'ingestion de certaines plantes (cassave, manioc…) et de noyaux de certains fruits. Ces derniers contiennent une molécule de cyanogène, l'amygdaline, décomposée dans l'intestin en glucose, aldéhyde et cyanure, sous l'effet des bêta-glucosidases. L'amande amère possédant elle-même une bêta-glucosidase activée à l'air, elle libère des effluves de cyanure d'hydrogène et de benzaldéhyde, c'est ce dernier qui dégage l'odeur d'amande amère couramment attribuée au cyanure lui-même.
La combustion de certains polymères (polyuréthanes) a entraîné des intoxications au cyanure et l'utilisation même des sels de cyanure en métallurgie en a accru le risque. Il est admis que, dans beaucoup d'incendies, notamment « feux de lits » (personnes fumant au lit, s'endormant, la cigarette provoquant une combustion lente des couvertures), les fumées peuvent contenir beaucoup de cyanures, ce qui explique que l'on trouve assez fréquemment des victimes décédées par intoxication avant d'être brûlées.
On trouve également du cyanure dans les pépins de pomme. Il est donc conseillé d'éviter d'ingérer ces derniers, même s'ils demeurent peu toxiques.
Antidotes
Les antidotes suivants existent :
- nitrite d'amyle associé au nitrite de sodium et au thiosulfate de sodium ;
- l'hydroxocobalamine, qui capte le cyanure pour conduire à la vitamine B12, atoxique et excrétée par les urines.
- sels de cobalt
Il est nécessaire de réagir vite et, en cas d'arrêt respiratoire, de faire respirer de l'oxygène et en aucun cas de pratiquer le bouche à bouche car il y a un risque d'intoxication à l'expiration. Sous l'action de la chaleur le cyanure ne représente aucun danger.
Nomenclature
Cyanure de sodium :
- numéro CAS : 151-50-8
- fiche toxicologique INRS : FT111
Cyanure de potassium :
- numéro CAS : 143-33-9
- fiche toxicologique INRS : FT111
Histoire
- À l'issue de la Seconde Guerre mondiale plusieurs nazis se sont suicidés en ingérant une capsule de cyanure, notamment Richard Glücks (1889-1945), Heinrich Himmler (1900-1945) et Hermann Göring (1893-1946) ; Magda Goebbels (1901-1945) et Joseph Goebbels, qui ont empoisonné au cyanure leurs six enfants et se sont suicidés, mais en se tirant une balle dans la tête.
- La tentative d'empoisonner Raspoutine au cyanure échoua, mais on ignore s'il avait eu recours à la mithridatisation ou si le cyanure avait réagi à la cuisson avec le sucre du gâteau où il avait été placé.
- 914 adeptes de la secte le Temple du Peuple sont décédés par absorption de cyanure lors d'un suicide collectif en 1978.