Carbone - Définition
La liste des auteurs de cet article est disponible ici.
Etymologie
Le nom carbone vient du latin carbo, carbōnis signifiant « charbon » de symbole germ.
Nucléosynthèse
L'élément carbone n'est pas directement issu du Big Bang (nucléosynthèse primordiale), car les conditions de sa formation n'étaient pas réunies (la dilatation et le refroidissement de l'univers ont été trop rapides).
Le carbone est en revanche produit en masse dans le cœur des étoiles très massives, dites de la branche horizontale, où trois noyaux d'hélium fusionnent (réaction triple alpha).
Historique
Le nom carbone n'apparaît dans le dictionnaire de l'Académie française, qu'à sa 6e édition (1832-5).
Préhistoire
Le carbone est présent sur terre depuis la formation de celle-ci : il a été produit par nucléosynthèse au coeur des étoiles qui ont explosé avant la formation du système solaire. Il existe sous forme de sédiments, charbon, pétrole, et également sous sa forme pure graphite, diamant. Les diamants naturels pouvant se trouver dans la kimberlite des cheminées d'anciens volcans, notamment en Afrique du Sud et dans l'Arkansas. On peut parfois trouver des diamants microscopiques dans certaines météorites.
Histoire
Elle est marquée par la considération accrue de l'importance du carbone.
- Deuxième millénaire (tradition de moines fondeurs, comme les Pères Chartreux, etc. - Elaboration (métallurgie) de fontes et aciers.
- Elaboration de la cémentation, « plus vieux » traitement connu en thermochimie.
- 1797 - Découverte de la forme « diamant » (voir article diamant synthétique).
- 1828 - Découverte des composés organiques et de la chimie organique (voir article Friedrich Wöhler).
- 1842 - Avec la RDM, August Wöhler pose les fondements de la future « science des matériaux ».
Chimie
Corps simple
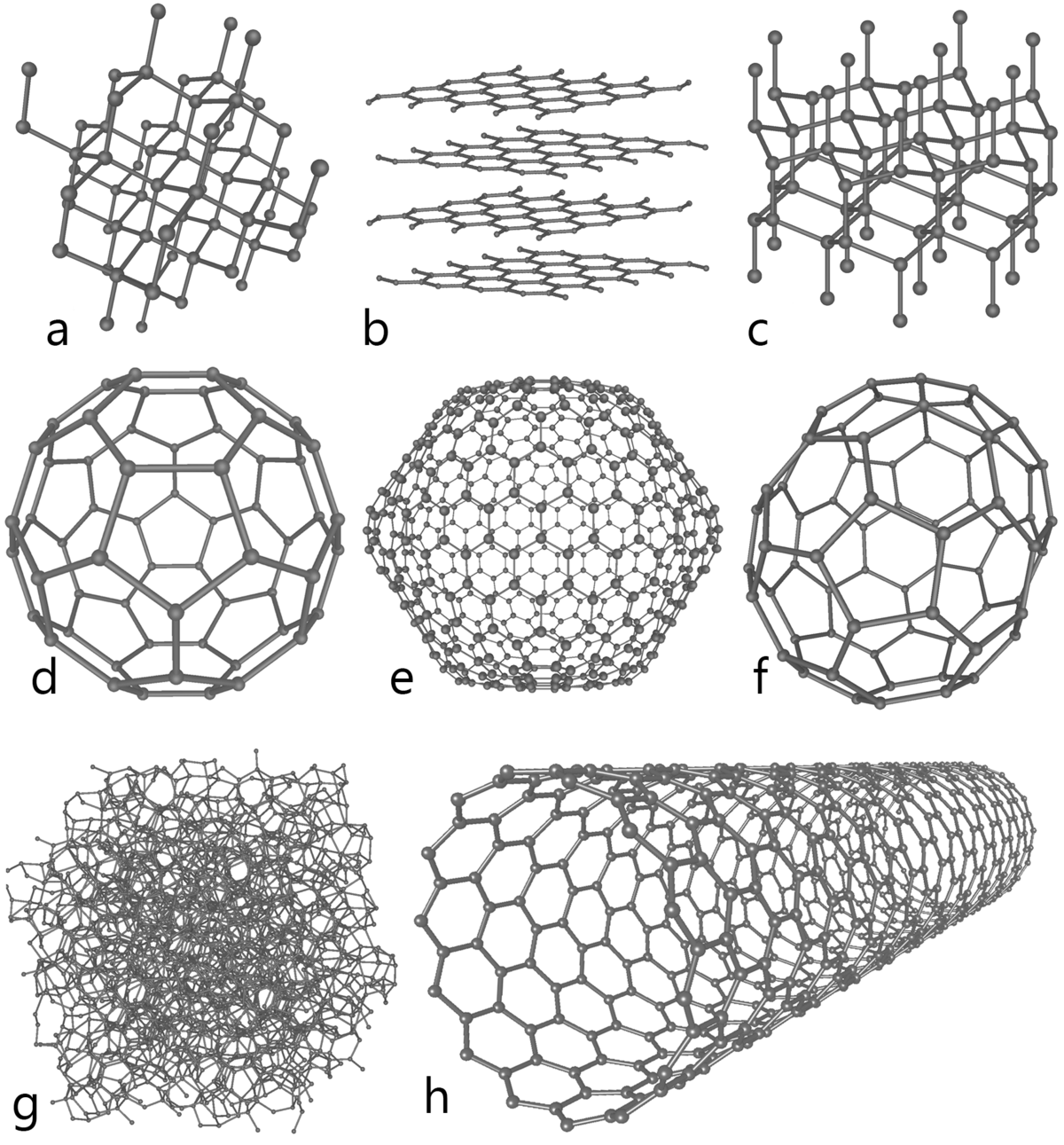 |  | |
| Huit formes du carbone : diamant, graphite, lonsdaléite, buckminsterfullerène et 2 autres fullerènes, amorphe, et nanotube de carbone | Le diamant et le graphite sont les deux formes allotropiques les plus répandues du carbone, elles diffèrent par leur aspect (en haut) et leurs propriétés. Cette différence est due à leur structure (en bas). |
Le carbone est présent dans la nature dans deux formes allotropiques principales :
- le graphite, empilement de structures cristallines hexagonales et monoplanes (graphènes, et de couleur grise. C'est la forme stable à température et pression ambiante.
- le diamant, de structure cristalline tétraédrique (structure type « diamant ») est transparent. C'est la forme stable à haute température et haute pression, métastable à température et pression ambiante.
Dans les conditions de pression normales, le carbone est sous la forme graphite, dans laquelle chaque atome est lié à trois autres dans une couche d'anneaux hexagonaux fusionnés, comme ceux des composés aromatiques hydrocarbonés. Grâce à la délocalisation des orbitales π, le graphite conduit l'électricité. Le graphite est mou, car les liaisons chimiques entre les plans sont faibles (2 % de celles des plans) et les couches glissent donc facilement les unes par rapport aux autres.
Sous très haute pression, le carbone cristallise dans un système cubique à face centrée nommé diamant, dans lequel chaque atome est lié à quatre autres (distance interatomique de 136 pm). Le diamant, grâce à la résistance des liaisons carbone-carbone, est, avec le nitrure de bore, la matière la plus dure à rayer. À température ambiante, la métamorphose en graphite est si lente qu'elle paraît invisible. Sous certaines conditions, le carbone se cristallise en lonsdaléite, une forme similaire au diamant mais hexagonale. De toutes les pierres précieuses, le diamant est la seule à se consumer complètement.
 | 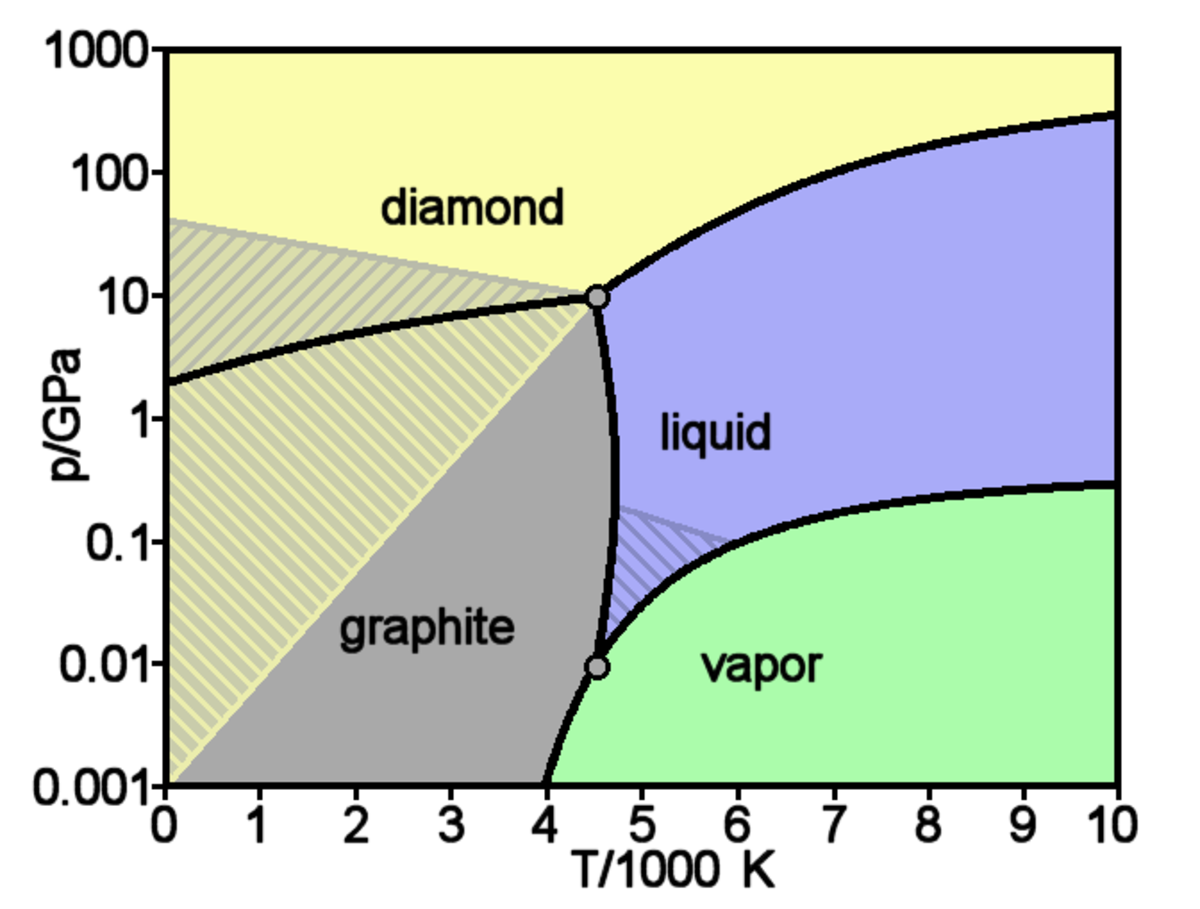 | |
| Le diamant, une des formes cristallines les plus recherchées du carbone | Diagramme de phases simplifié du carbone : phases en fonction de la pression et de la température. |
En plus du graphite (pur sp2) et du diamant (pur sp3), le carbone existe sous forme amorphe et hautement désordonnée (a-C). Ces formes amorphes du carbone sont un mélange de sites à trois liaisons de type graphite ou à quatre liaisons de type diamant. De nombreuses méthodes sont utilisées pour fabriquer du a-C : pulvérisation, évaporation par faisceau d'électrons, dépôt à l'arc électrique, ablation laser...
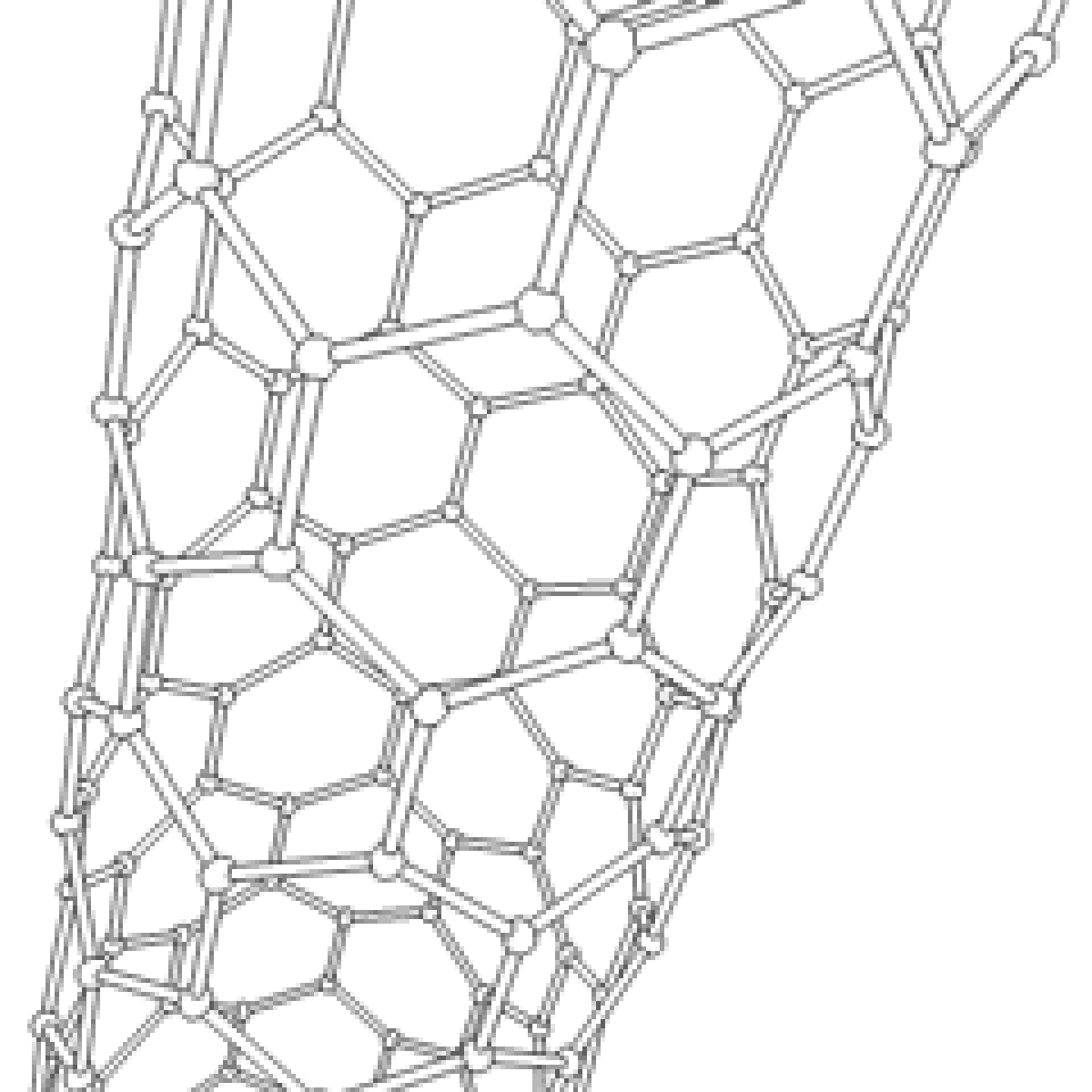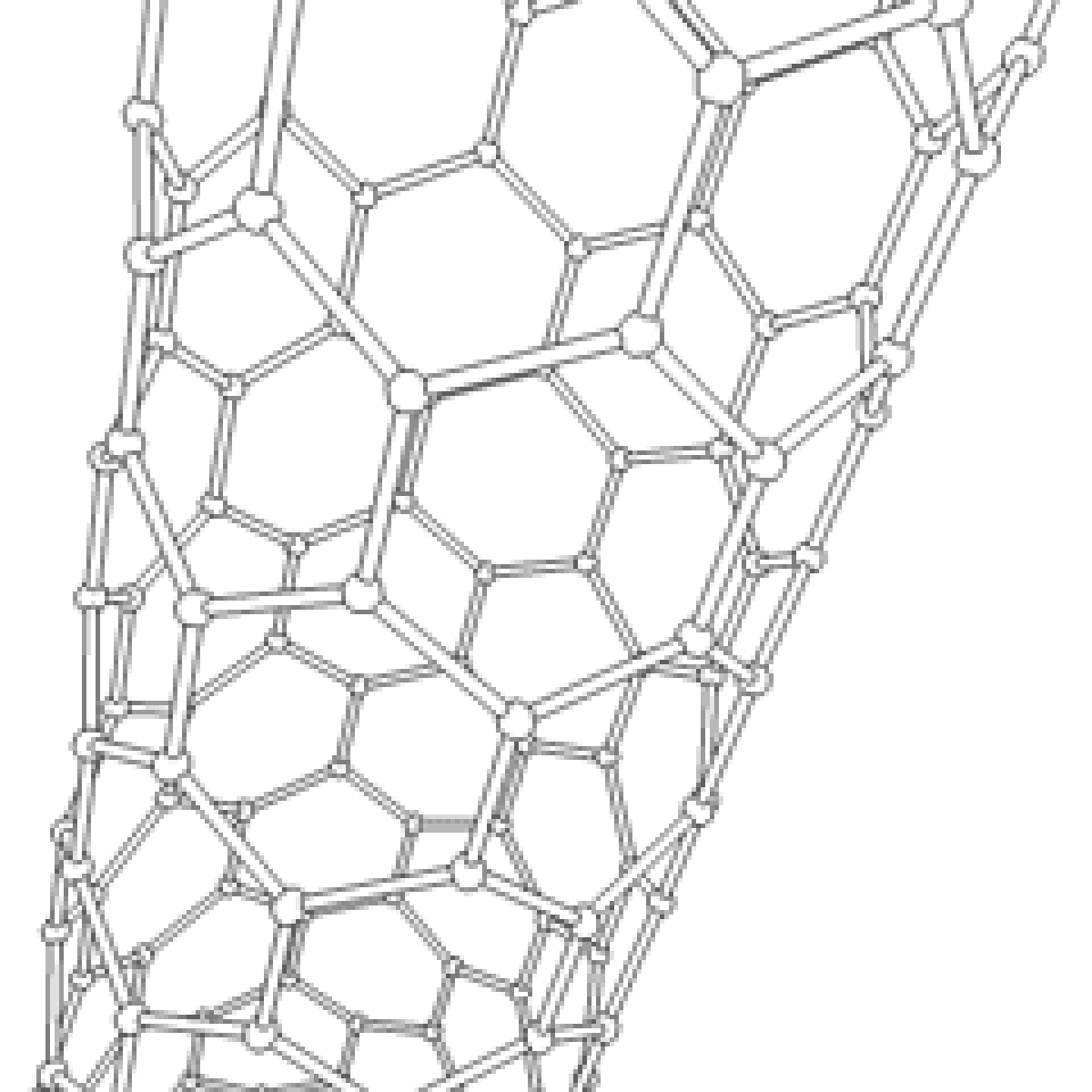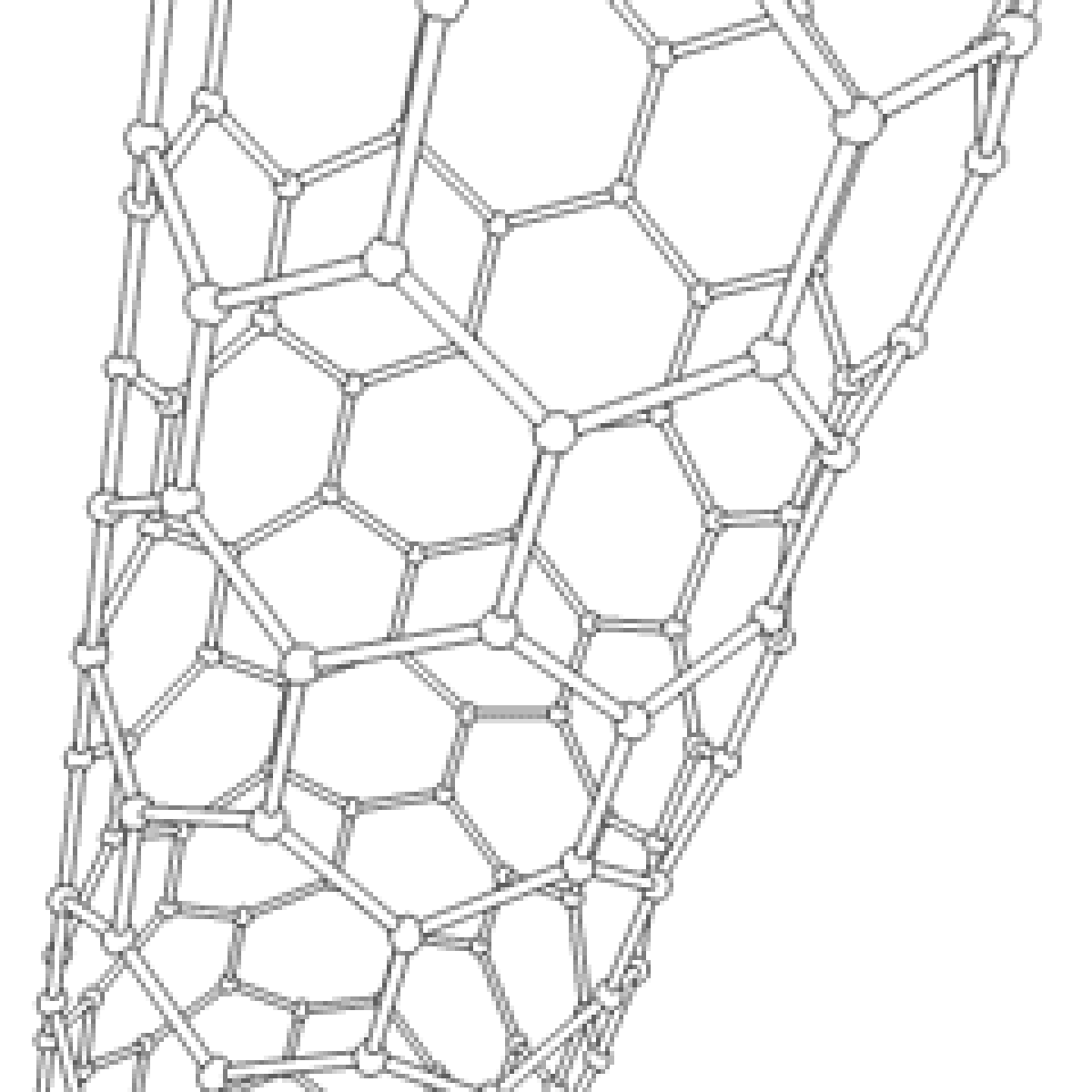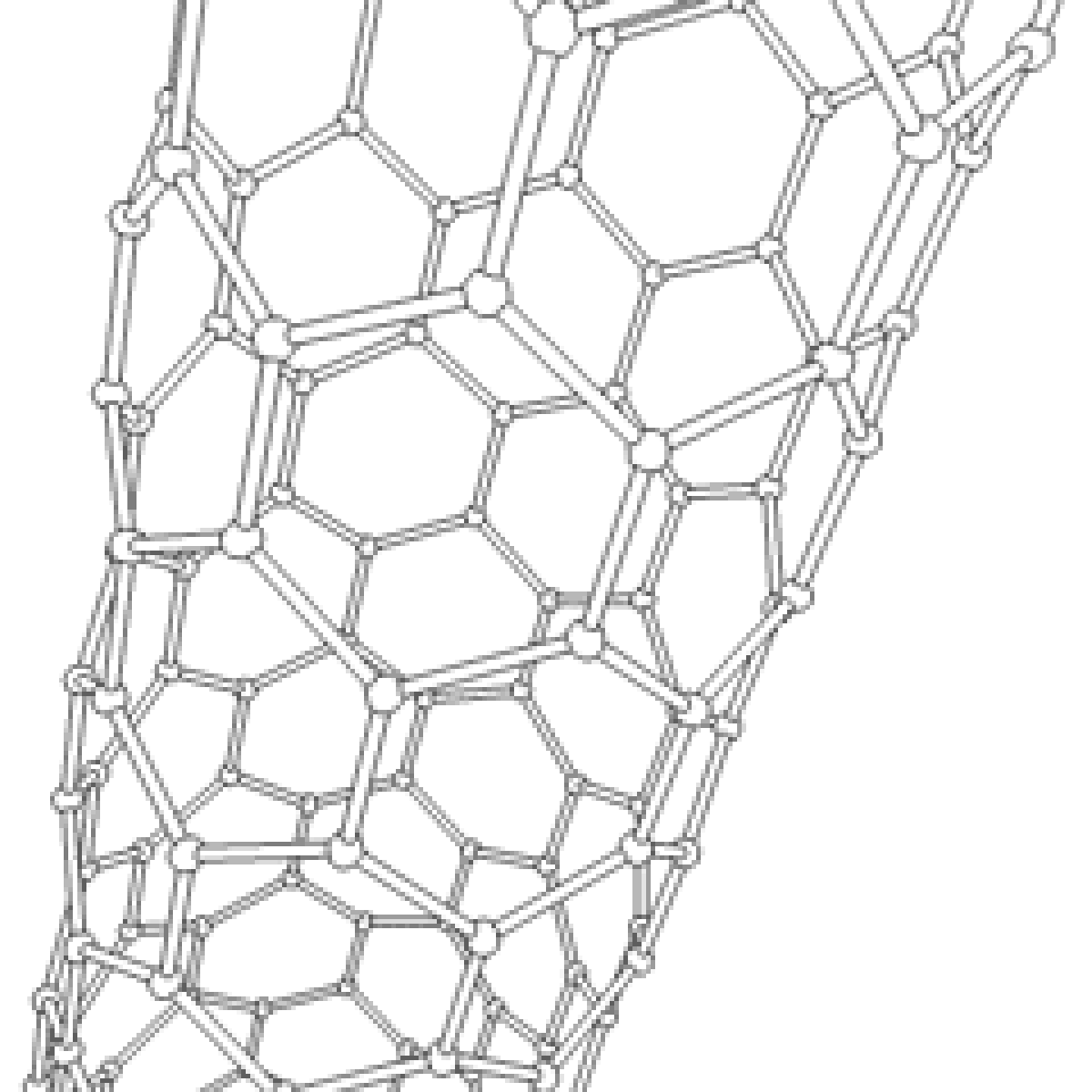
Le carbone se sublime à 5 100 K. Sous forme gazeuse, il se constitue habituellement en petites chaînes d'atomes appelées carbynes. Refroidies très lentement, celles-ci fusionnent pour former les feuilles graphitiques irrégulières et déformées qui composent la suie. En particulier, parmi ces dernières, on trouve des formes où les feuilles sont pliées dans une forme stable et close comme une sphère ou un tube, appelées fullerènes, comme le buckminsterfullerène, C. Certaines de ces formes sont aussi connues sous le nom de « footballène » et ont des propriétés qui n'ont pas encore été toutes analysées, mais apparaissent comme des structures extrêmement rigides.
Les formes cylindriques du carbone sont appelées nanotubes et ont été découvertes dans le culot se formant à la cathode de l'arc électrique durant la synthèse de fullerènes. Ces objets de diamètre nanométrique et de longueur atteignant parfois le millimètre se présentent comme des couches de graphène enroulées sur elles-mêmes.
Les nanotubes fabriqués par la méthode de l'arc électrique sont presque tous « multifeuillets ». Conjointement à ces nanotubes, on observe un grand nombre de nanoparticules polyédriques. Les observations en microscopie électronique en transmission haute résolution ((en) HRTEM : High-resolution Transmission Electron Microscopy) révèlent que ces nanoparticules de carbone sont constituées de plusieurs couches de graphène, fermées, laissant une cavité nanométrique en leur centre. Les nanotubes de carbone sont d'excellents dopants mécaniques utilisés pour les ailes d'avions, par exemple afin d'améliorer leur dureté tout en conservant une bonne flexibilité.
Et enfin, les oignons de carbone sont à la base des fullerènes multicouches.