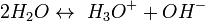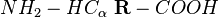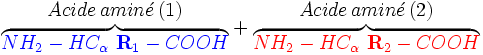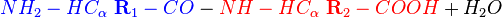Biochimie - Définition
La liste des auteurs de cet article est disponible ici.
Sous-disciplines de la biochimie
- Biochimie structurale
- Biochimie métabolique
- Biochimie génétique
- Biochimie fonctionnelle
- Biochimie médicale et clinique
Biomolécules
L'eau

L'eau est le constituant principal des êtres vivants. Chez l'être humain cette molécule représente de 55 à 75% de la masse corporelle (mais varie selon la croissance et l'environnement). Certaines des caractéristiques de l'eau font d'elle une molécule remarquable, aux particularités qui ont permis à la vie sur Terre de se développer. Ces caractéristiques sont surtout liées à sa nature dipolaire.
- L'eau a une force de cohésion élevée grâce aux liaisons hydrogène, ce qui rend cette matière difficile à évaporer (température d'ébullition particulièrement élevée pour une molécule de cette masse molaire). Cela permet à une importante phase liquide d'exister aux températures connues sur Terre, phase liquide indispensable à la vie telle que nous la connaissons.
- De même, ses propriétés de solvant "doux" permettent à un très grand nombre de réactions biochimiques de se produire. L'eau est particulièrement un excellent solvant pour les solutés polaires ou ioniques. L'eau est en effet capable d'entourer et de séparer les particules chargées en formant des sphères de solvatation.
- L'eau peut former des liaisons hydrogène avec certains atomes composant les biomolécules (la liaison hydrogène avec l'acide carboxylique des lipides explique la tête hydrophile des lipides, les liaisons hydrogène ont une influence sur la structure spatiale des protéines).
- L'eau se dissocie naturellement en ion oxonium (ou hydronium) H3O+ et ion hydroxyde OH-.
Le pH de l'eau varie donc en fonction du rapport entre ces deux ions, cette propriété influant fortement sur des molécules telles que les enzymes. Certaines enzymes digestives agissent dans l'estomac (au pH acide proche de 2) et sont inactivées dans l'intestin (au pH basique proche de 8) [exemple : le Coca a un pH de 4 et le citron de 3].
- L'eau est impliquée dans la plupart des réactions biochimiques, car c'est le solvant principal et essentiel pour que ces réactions aient lieu.
- Enfin elle est fortement utilisée en biochimie pour faire des dilutions et obtenir des solutions avec certaines particularités (solutions tampon).
On peut aussi signaler l'importance de l'eau pour la vie dans son aspect général :
- Le fait que la densité de l'eau soit plus grande à l'état liquide que solide, propriété commune avec le bismuth, a une conséquence remarquable : la glace flotte sur l'eau ! En règle générale, la densité à l'état liquide est plus faible qu'à l'état solide pour les autres corps).
De surcroît, le fait que la densité de l'eau soit maximale à 4 °C fait que la température au fond d'un lac ne peut pas descendre en dessous de 4 °C (sauf cas extrêmes). Cela permet à la vie aquatique de survivre aux périodes glacées, car l'eau reste liquide sous son manteau de glace isolante. - Par ailleurs, sa tension superficielle particulièrement élevée permet le phénomène de capillarité, qui permet, entre autres, aux plantes de pousser et à de nombreux êtres vivants de se déplacer sur la surface de l'eau.
Les glucides (hydrates de carbone)

Les glucides ou sucres sont des composés polyfonctionnels qui ont pour formule globale Cn(H2O)n, d'où leur nom d'hydrates de carbone.
Les sucres, plus correctement appelés oses, jouent un rôle majeur dans le métabolisme énergétique, c'est-à-dire la production d'énergie chimique qui sera utilisée au cours des réactions d'anabolisme. Ils sont également très importants dans d'autres processus métaboliques tels que la synthèse d'acides nucléiques, les processus d'hydroxylation et la synthèse de cérébrosides et de glycoprotéines. Les glucides interviennent aussi dans le transfert des cations dans l'intestin et dans des mécanismes de détoxification tels que la glycuroconjugaison, l'excrétion d'ammoniac et l'épuration de l'hydrogène.
Chez les bactéries, ils sont une partie importante de la membrane externe appelée paroi. Chez certaines bactéries, les lipides étant en quantité négligeable, l'assemblage de ces oses donne le peptidoglycane résistant à l'alcool. Chez d'autres, ils sont conjugués à des lipides, formant les lipopolysaccharides, ou LPS. Ils sont responsables des réactions immunitaires d'un organisme lorsque celui-ci est exposé à une entrée bactérienne. Ils jouent aussi un rôle important comme déterminant antigénique à la surface des cellules eucaryotes. Ils déterminent les groupes sanguins et sont une part importante du complexe majeur d'histocompatibilité, ou CMH.
Classification des glucides
Par nombre de résidus
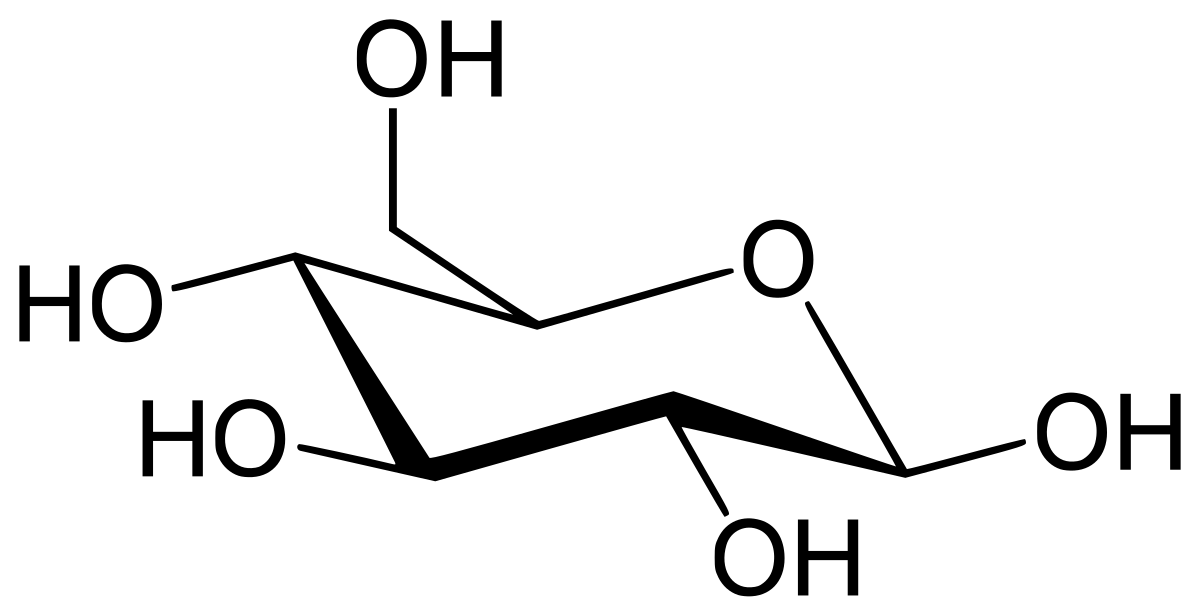
- Les molécules de glucides simples sont appelés oses ou monosaccharides (par exemple glucose, fructose et galactose).
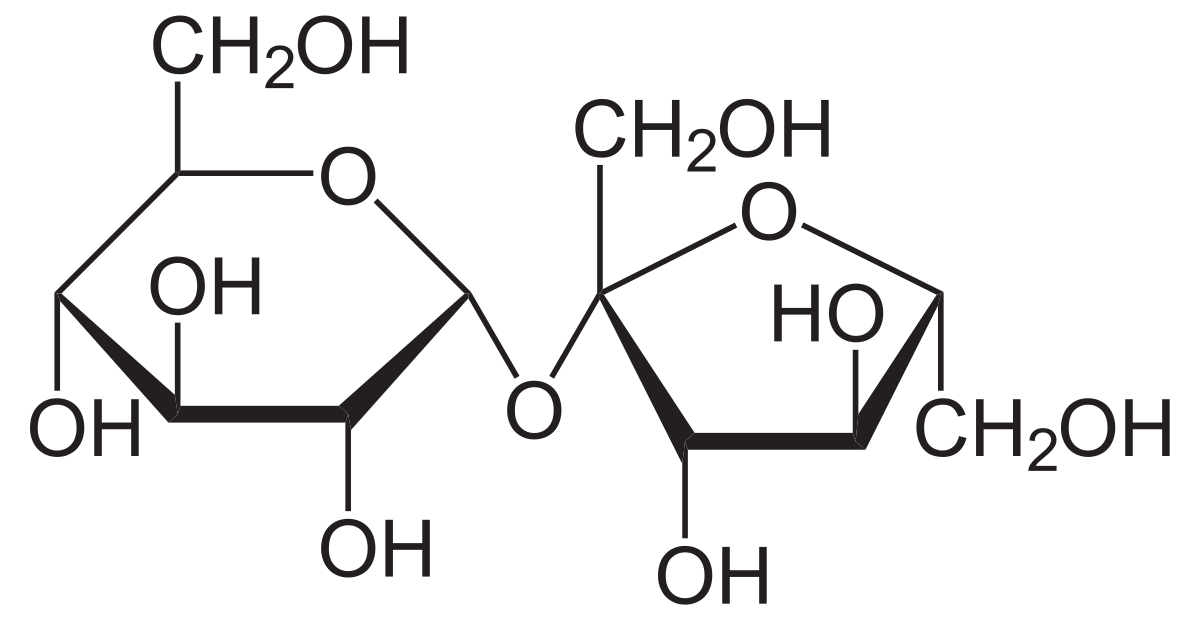
- Les glucides composés de deux résidus sont des diholosides ou disaccharides (saccharose, lactose). Il existe des enchaînements de plus de deux oses.
- Les oligosaccharides comprennent au plus dix résidus de monosaccharides et les polysaccharides, plus de dix. Les polysaccharides sont donc des polymères de plusieurs unités osidiques et jouent un rôle important dans le stockage de l'énergie (amidon, glycogène) ainsi que dans la structure des tissus végétaux (cellulose, chitine).
Par groupement chimique
Parmi les glucides on distingue les aldoses et les cétoses :
- les aldoses sont composés d'une chaîne d'alcools secondaires ayant à une extrémité un alcool primaire et un aldéhyde à l'autre extrémité. Ces derniers présentent une énantiomérie (séries L et D).
- Les cétoses possèdent une fonction cétone dans leurs chaînes, les autres carbones étant porteur d'une fonction alcool primaire ou secondaire selon la position.
Par nombre d'atomes de carbone
Les oses sont classés aussi par leur nombre d'atomes de carbone de la manière suivante: C3 trioses, C4 tétroses, C5 pentoses, C6 hexoses, C7 heptoses.
Exemples
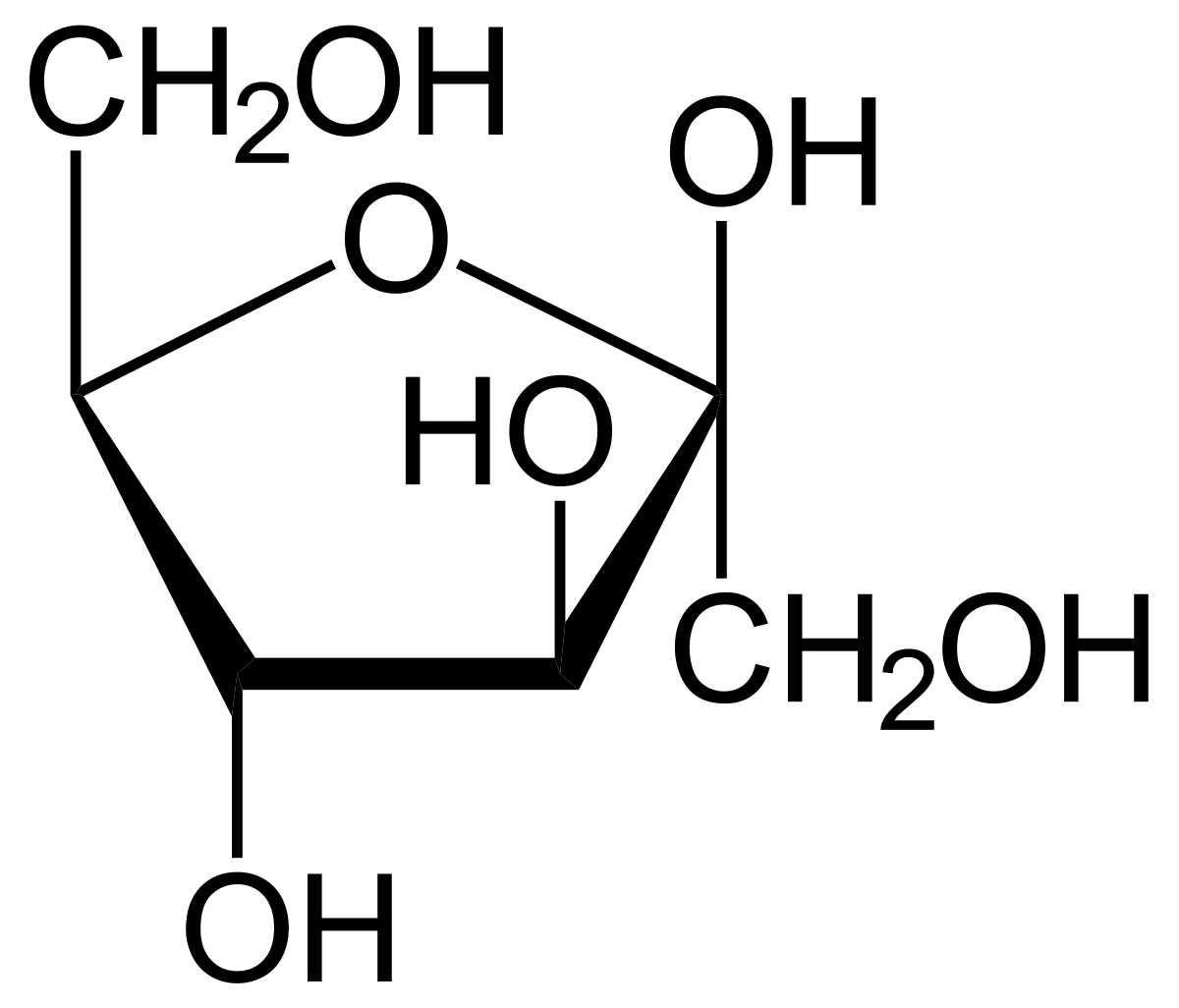
- Le glycéraldéhyde est l'ose le plus simple dans la classe des aldoses, c'est un aldotriose (C3). De même pour la dihydroxyacétone dans la classe des cétoses (cétotriose). Le ribose est un aldopentose (C5) qui entre dans la composition des acides nucléiques.
- Le glucose («gluco», du grec glukus, saveur sucrée) est un aldohexose de formule C6H12O6. On le trouve dans les fruits mûrs, le nectar des fleurs, la sève, le sang et certains sirops.
- Le fructose (du latin fructus, fruit) appelé aussi lévulose, est un cétohexose. On le rencontre dans les fruits, le miel, dans certaines boissons sucrées et dans les sécrétions séminales.
- Le saccharose (du grec sakkharon, sucre) de formule C12H22O11 est un disaccharide qui donne par hydrolyse du glucose et du fructose. Il se trouve dans la plupart des végétaux et en particulier dans la betterave sucrière, la canne à sucre.
- Le maltose est un disaccharide qui donne par hydrolyse deux molécules de glucose.
- Le lactose est un disaccharide qui donne par hydrolyse un glucose et un β-galactose. Le lactose est retrouvé notamment dans le lait et les produits laitiers.
Lipides
Définition
Les lipides, du grec « lipos » (« graisse »), constituent une classe assez hétérogène de molécules. Sont regroupées sous cette dénomination les molécules ayant un caractère hydrophobe marqué, c'est-à-dire très peu solubles dans l'eau mais solubles dans la plupart des solvants organiques, comme le chloroforme, par exemple. Nous trouvons aussi des lipides dans la cire de bougie, les graisses animales, l'huile d'olive et pratiquement tous les corps gras. La biochimie a complété cette définition en montrant que les lipides possédaient des voies de synthèse communes. Cependant, il n'existe pas encore de définition unique d'un lipide reconnue par l'ensemble de la communauté scientifique. Ceci tient probablement au fait que les lipides forment un ensemble de molécules aux structures et aux fonctions extrêmement variées dans le monde du vivant.
D'un point de vue métabolique, les lipides constituent des réserves énergétiques. Les sucres sont par exemple transformés en lipides et stockés dans les cellules adipeuses en cas de consommation supérieure à l'utilisation.
Les lipides, en particulier les phospholipides, constituent l'élément majeur des membranes cellulaires. Ils définissent une séparation entre le milieu intracellulaire et le milieu extracellulaire. Leur caractère hydrophobe rend impossible le passage de molécules polaires ou chargées, comme l'eau et les ions, car ils forment des groupements très compacts issus de liaisons covalentes faibles appelées interaction hydrophobe. Seules voies de passage possible : les protéines membranaires où, par exemple, les ions entrent et sortent de la cellule par le biais de canaux ioniques.
Plusieurs hormones sont des lipides, en général dérivées du cholestérol (progestérone, testostérone, etc.), ce qui permet d'agir comme filtre aux entrées des cellules. Les vitamines liposolubles peuvent aussi être classées parmi les lipides.
Contrairement aux acides nucléiques ou aux protéines, les lipides ne sont pas des macromolécules constituées d'une succession d'unités de base.
Structure et classification
Les lipides peuvent être classés selon la structure de leur squelette carboné (atomes de carbone chaînés, cycliques, présence d'insaturations, etc.):
- les acides gras : il s'agit d'acides carboxyliques à longue chaîne carbonée pouvant être saturée, insaturée, ramifiée, etc. Des exemples bien connus sont les oméga-3 et -6, mais aussi les prostaglandines.
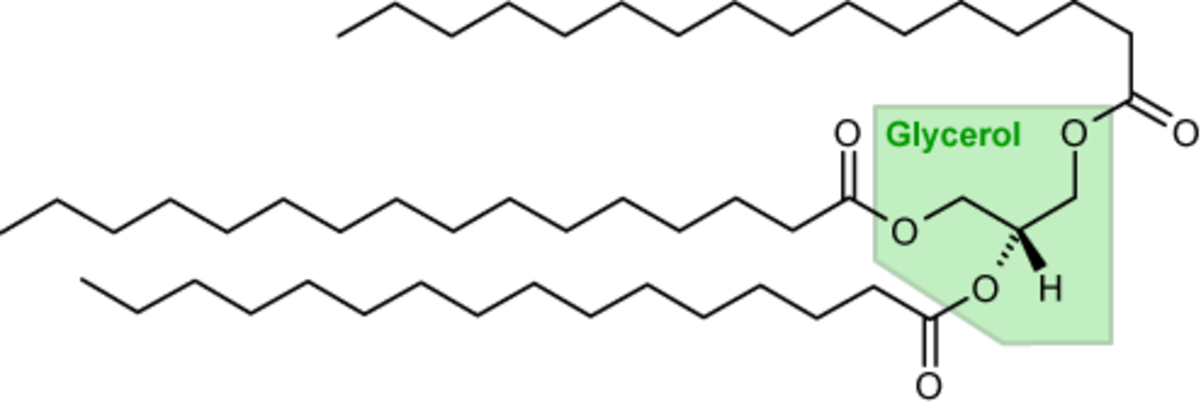
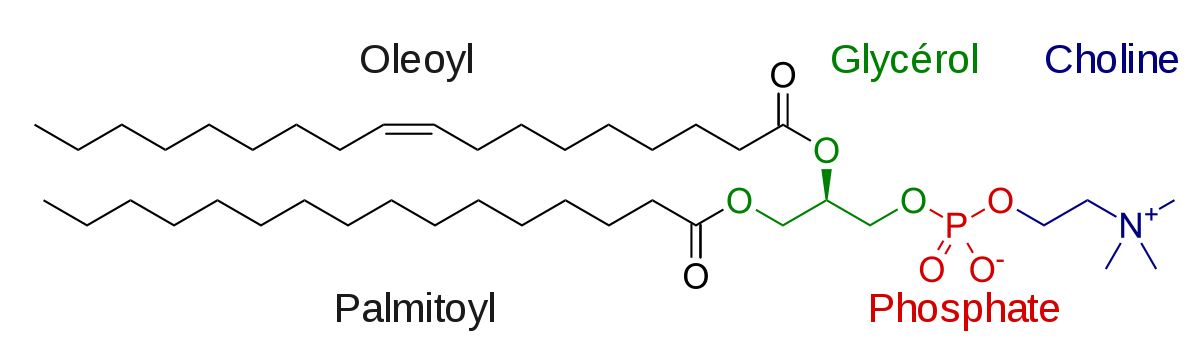
- les acylglycérols et phosphoacylglycérols : ces lipides sont formés par estérification d'un glycérol et d'un à trois acides gras (ou mono-, di- et triglycérides). Dans le cas des phosphoacylglycérols, l'estérification se fait avec glycérol, un ou deux acides gras et un phosphate. Le groupe phosphate peut à son tour subir une estérification par différents composés hydroxylés comme la choline ou la sérine. On obtient alors de la phosphatidylcholine et de la phosphatidylsérine, respectivement. Il est à noter qu'acylglycérols et phosphoacylglycérols sont également connus sous les noms de glycérides et phosphoglycérides.
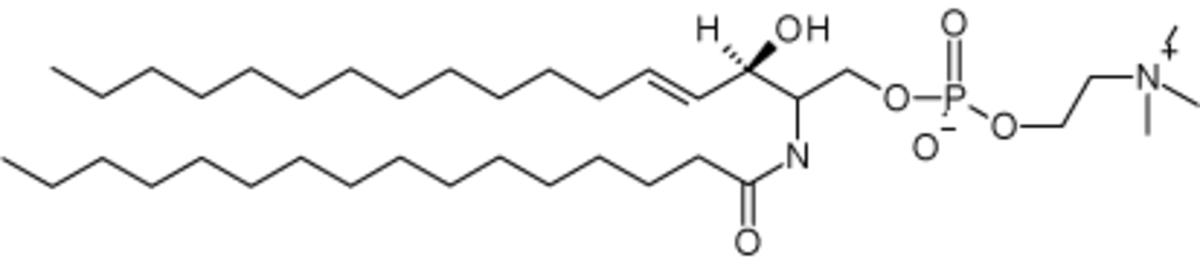
- les sphingolipides : ces lipides résultent de l'estérification puis de l'amidification de la sérine par deux acides gras. Une sous-classe bien connue de sphingolipides est celle des céramides.
- les stérols : les stérols sont des lipides possédant une chaîne carbonée plusieurs fois cyclisée. Ils ne sont donc pas linéaires comme les acides gras. Des exemples bien connus de stérols sont le cholestérol, la vitamine D et les hormones stéroïdiennes (testostérone, œstrogènes, cortisone).
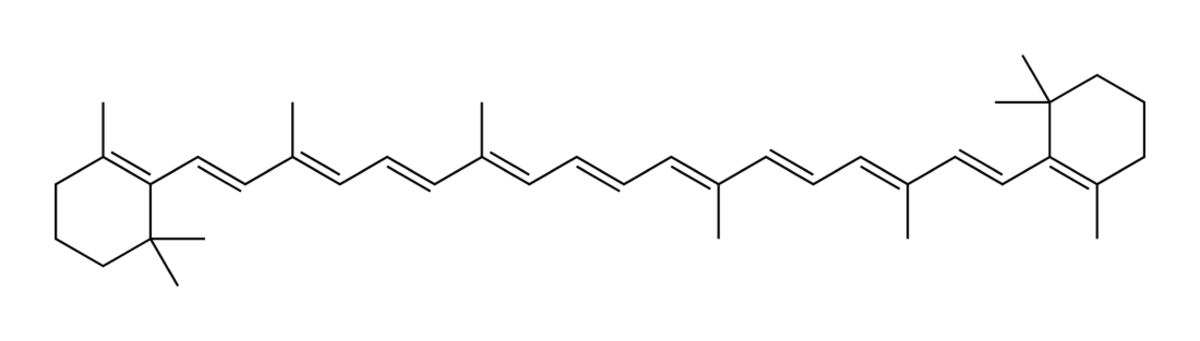
- les prénols : il s'agit de lipides dérivant de l'isoprène, comme par exemple les vitamines E et K ou le β-carotène.
- les polykétides : ils forment une gamme très vaste de composés naturels dont sont dérivés de nombreux antibiotiques comme les macrolides.
- les saccharolipides : ils résultent de l'estérification et/ou de l'amidification de sucres et d'acides gras. L'exemple le plus connu de saccharolipide est sans doute le lipopolysaccharide.
Pour des raisons pratiques et historiques, acylglycérol et phosphoacylglycérol sont souvent considérés comme deux catégories différentes, de même que phosphoacylglycérol et phosphosphingolipide peuvent être regroupés sous l'appellation de phospholipides.
| cholestérol | 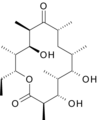
macrolide | 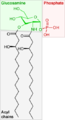
saccharolipide précurseur du lipopolysaccharide |
Protéines (protides)
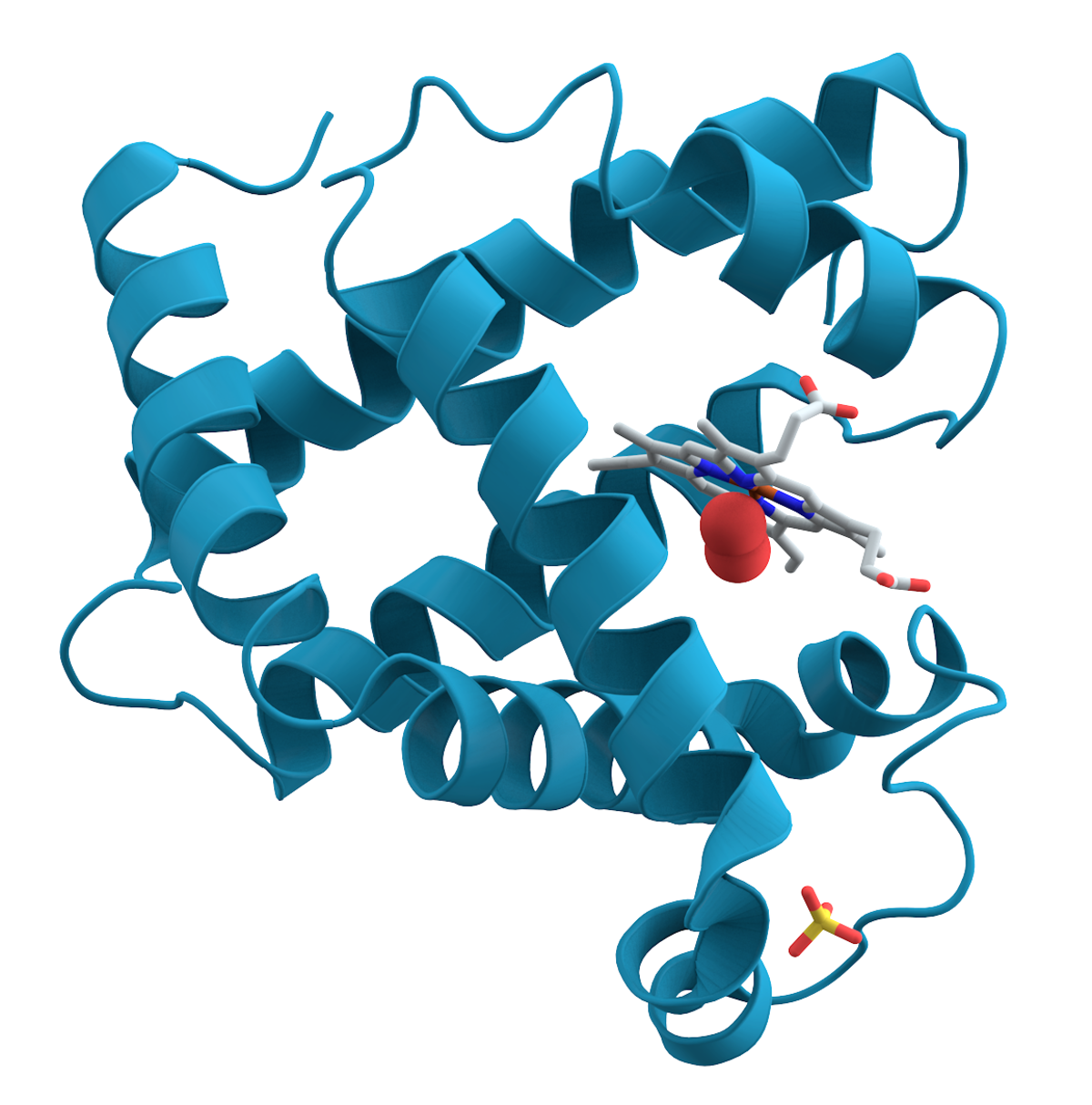
Les protéines (du grec prôtos, premier) sont des polymères composés d'une combinaison de quelques 20 acides aminés. La plupart des protéines sont formées de l'union de plus de 100 acides aminés (résidus) reliés entre eux par des liaisons peptidiques. Pour un nombre moins important de résidus on parle de peptides (< 50 résidus) et de polypeptides (≥ 50 résidus).
Acides aminés
Les acides aminés (« amin » du grec ammôniakos, ammoniac) sont des composés organiques azotés qui possèdent une formule générale du type :
L'atome de carbone central Cα (carbone alpha) est relié à un groupement amine (NH -), à un groupement carboxyl acide (- COOH) et à un radical R variable d'un acide aminé à un autre. Les radicaux (R) peuvent avoir des propriétés différentes, certains sont hydrophiles, d'autres hydrophobes. Certains, en solution aqueuse, s'ionisent positivement (basiques) et d'autres négativement (acides) ou restent neutres. Les mammifères possèdent les enzymes nécessaires pour la synthèse de l'alanine, l'asparagine, l'aspartate, la cystéine, le glutamate, la glutamine, la glycine, la proline, la sérine, et la tyrosine. Quant à l'arginine et l'histidine, ils sont produits mais en quantité insuffisante surtout pour les jeunes individus. En revanche, l'isoleucine, la leucine, la lysine, la méthionine, la phénylalanine, la thréonine, le tryptophane, et la valine ne peuvent pas être fabriqués par notre organisme. Au risque de déficit, ils doivent être apportés régulièrement par l'alimentation dans les bonnes proportions : ce sont les acides aminés essentiels.
Structure des protéines
Les acides aminés peuvent se lier les uns aux autres par une liaison peptidique au cours de la synthèse protéique dans les ribosomes. La liaison peptidique se fait entre le groupement acide (COOH) d'un acide aminé et le groupement amine (NH2) de l'autre :
la réaction produit un di-peptide :
Dans la cellule, cette réaction est catalysée par la peptidyl transférase, elle nécessite l'hydrolyse d'ATP (source d'énergie) et la présence d'ions magnésium. Pour chaque liaison formée, une molécule d'eau est formée.
La séquence des acides aminés d'une protéine (l'arrangement et l'ordre des résidus) constitue la structure primaire. Par exemple, pour construire un peptide de 10 résidus à l'aide de la collection de 20 acides aminés on dispose de 2010possibilités (soit 1 suivi de 13 zéros !). En solution aqueuse, comme on a dit, les radicaux possèdent des propriétés chimiques différentes. Certains radicaux peuvent former des liaisons chimiques plus ou moins fortes avec d'autres radicaux de la même chaîne peptidique. Certains se repoussent et d'autres se rapprochent et forment des liens chimiques. La chaîne d'acides aminés aura donc tendance à se replier sur elle-même pour adopter une structure tridimensionnelle précise. Et cette structure tridimensionnelle dépend avant tout de la séquence des acides aminés formant la chaîne. En effet, 4 grands types d'interactions interviennent dans le repliement de la chaîne peptidique :
- L'effet hydrophile / hydrophobe,
- Les forces de Van der Waals,
- Les liaisons ioniques,
- Les liaisons hydrogène,
Ces 4 premiers types d'interactions sont considérés comme étant faibles (forts lorsque nombreux cependant)
- Les ponts disulfure (liaison covalente entre les atomes de soufre qui relient deux cystéines éloignées l'une de l'autre sur la chaîne). Cela constitue une interaction forte.
Ainsi certaines parties de la chaîne peptidique adoptent une structure régulière appelée structure secondaire. On en reconnaît, selon les angles de torsion des liaisons, 3 grands types :
- L'hélice α : la chaîne peptidique prend la forme d'une spirale. Les différentes spires sont stabilisées par des liaisons hydrogène tous les 4 résidus (liaisons hydrogènes dites "intracaténaires").
- Le feuillet β : il se forme des liaisons hydrogène entre certains segments (brins β) de la chaîne peptidique disposés parallèlement les uns par rapport aux autres (les liaisons hydrogènes sont dites "intercaténaires"). L'ensemble forme comme un feuillet plissé.
- Le coude ou « turn » : c'est une structure moins ordonnée qui forme généralement un lien court entre des structures ordonnées (hélice-hélice, feuillet-feuillet ou feuillet-hélice). Une boucle est un lien plus long.
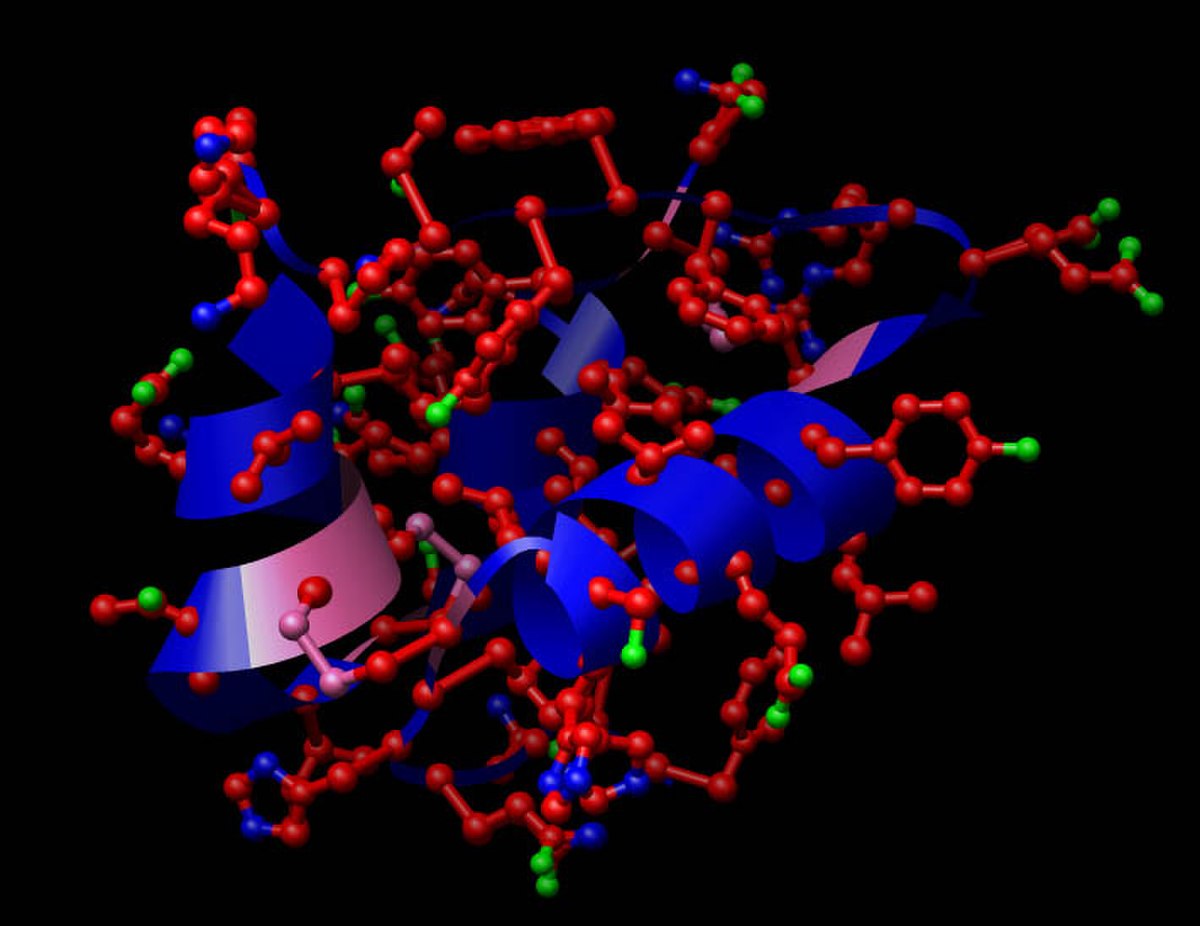
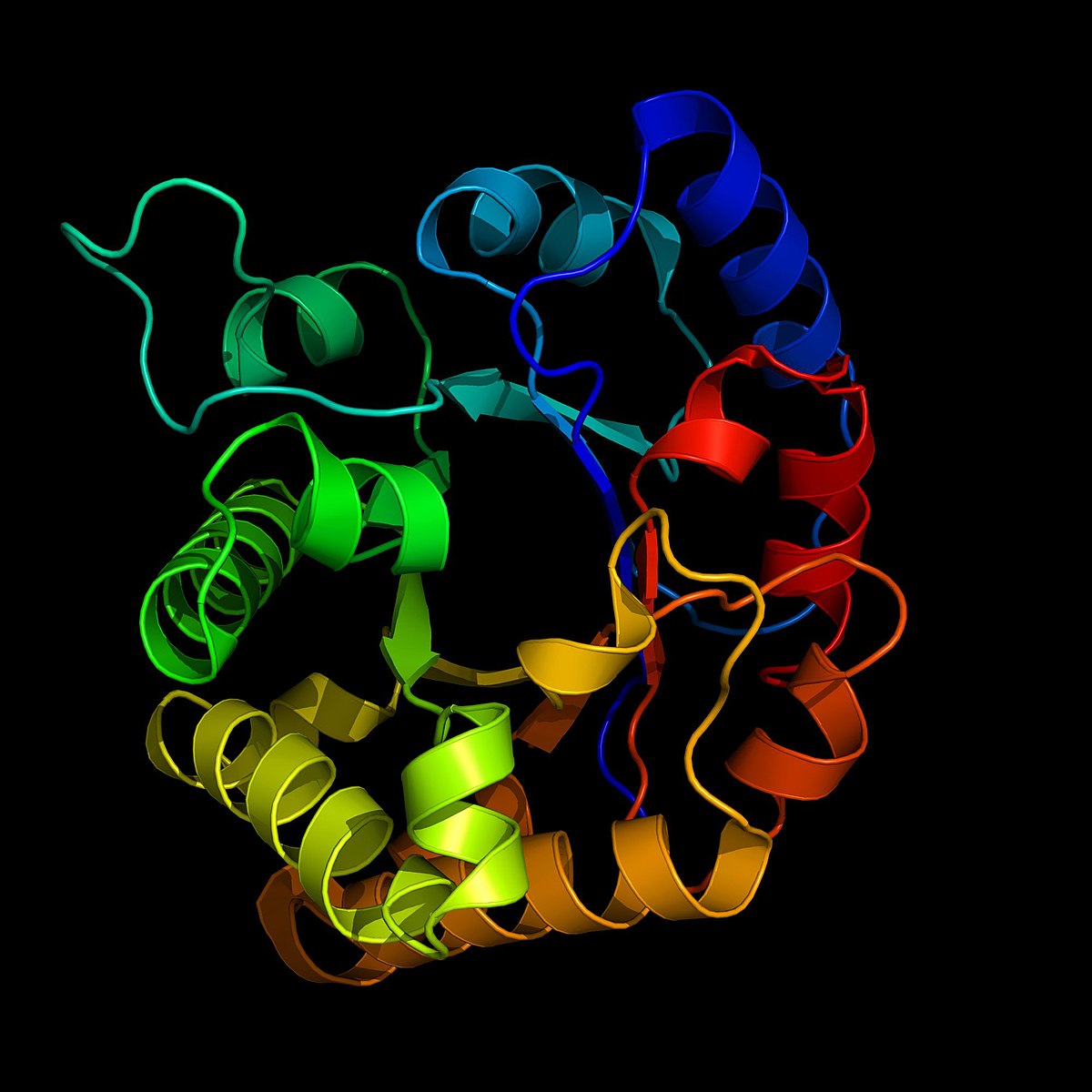
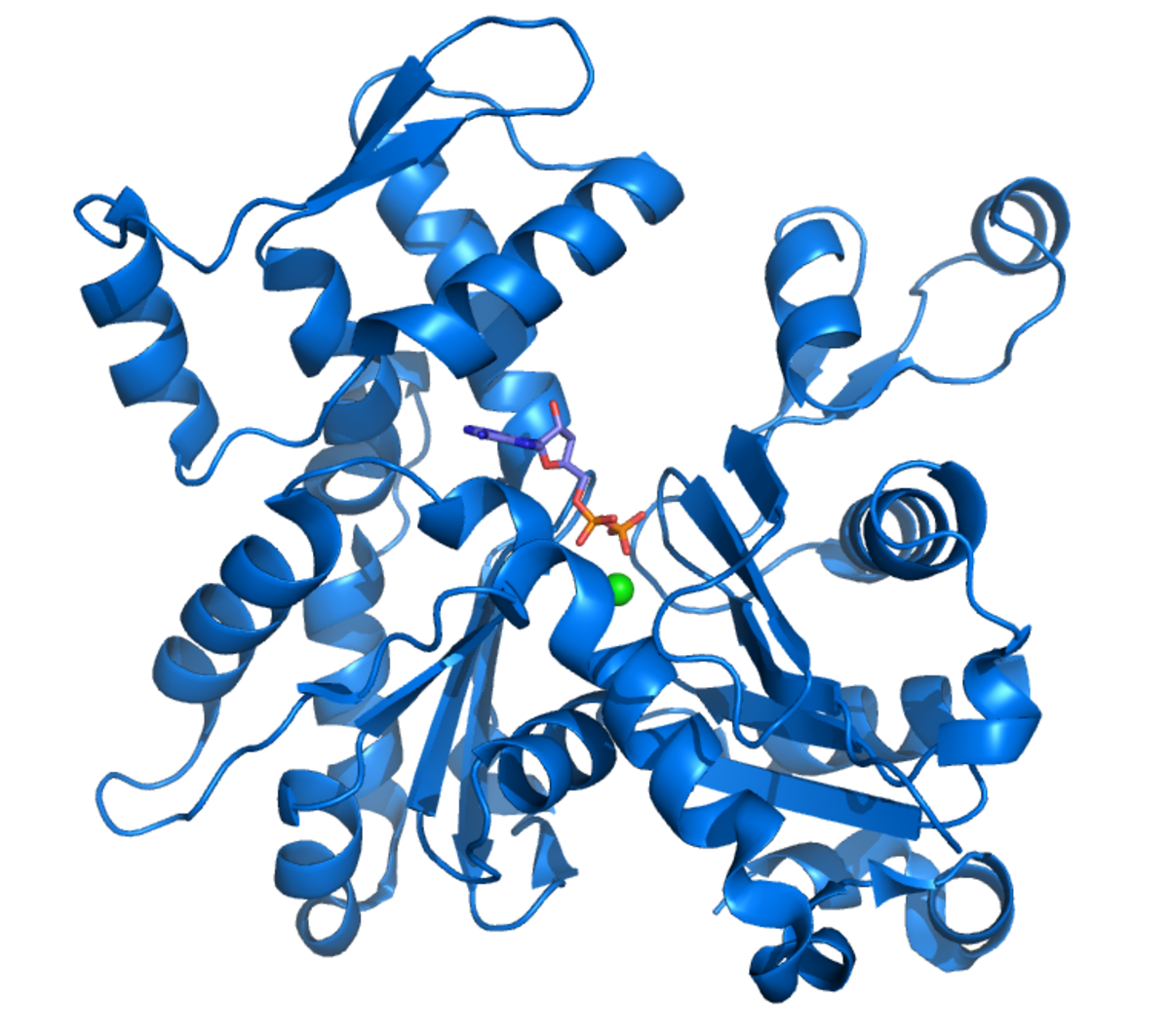
La forme finale de la chaîne peptidique, c’est-à-dire la structure tridimensionnelle qu'adopte la chaîne d'acides aminés, constitue la structure tertiaire de la protéine (Voir la figure de la myoglobine en 3D).
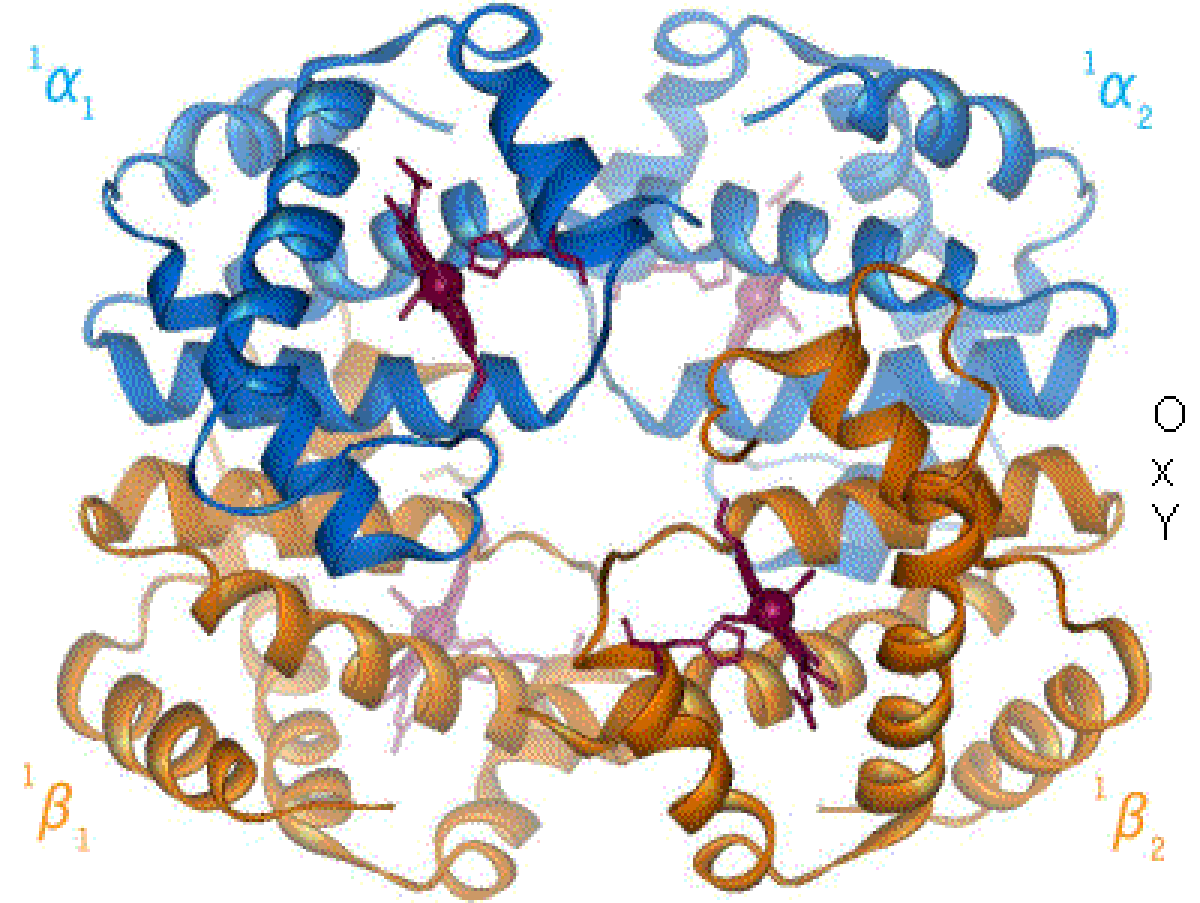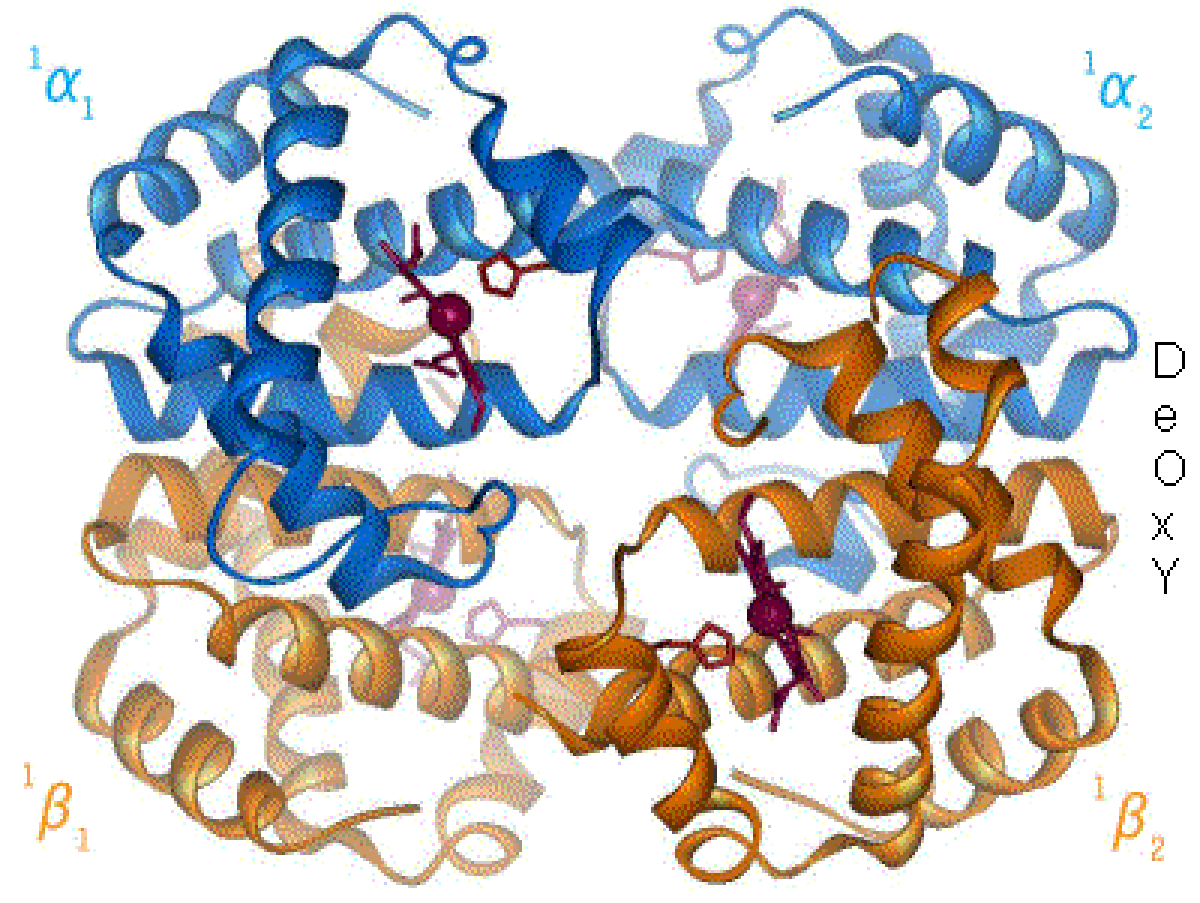
Certaines protéines, plus complexes, résultent de l'assemblage des différentes chaînes (monomères) ce qui constitue la structure quaternaire de la protéine. Par exemple, l'hémoglobine est formée de l'association de 4 chaînes peptidiques.
La structure de la protéine peut être dénaturée par plusieurs facteurs notamment: la température, les pH extrêmes et l'augmentation de la force ionique dans le milieu ou par des agents chimiques dénaturants (2-mercaptoéthanol). La dénaturation de la structure 3D d'une protéine s'ensuit généralement par la perte de sa fonction. On parle de relation structure-fonction.
Fonctions
Les protéines assurent plusieurs fonctions au sein des cellules et de l'organisme, qui sont à l'essence même de la vie. En voici une liste non exhaustive avec quelques exemples :
- Structure et soutien : tubuline, élastine, collagène, kératine.
- Catalyse des réactions biologiques : enzymes.
- Transport et stockage : hémoglobine, ferritine.
- Signalisation et régulation : hormones peptidiques, cytokines.
- Réception et transduction des signaux : récepteurs biologiques.
- Mouvement et motricité : système actine / myosine.
- Identité et défense contre les agressions biologiques : anticorps.
- Protection contre le stress environnemental : les chaperonnes.
- Détoxification : cytochrome P450, peroxydases, superoxyde dismutase.
| Insuline (hormone). | Triosephosphate isomérase (Enzyme). | ||
Rhodopsine (récepteur). | F actine, polymère (protéine de soutien/ protéine motrice). | Collagène (protéine de soutien). |
Protéome
Pour un total d’environ 20 000 à 25 000 gènes (génome), on estime à un million le nombre de protéines différentes qui peuvent être produites dans les cellules humaines (protéome). Le nombre de protéines produites par le cerveau humain, dont le rôle est essentiel pour son fonctionnement, est estimé à environ 12 000.
Acides nucléiques
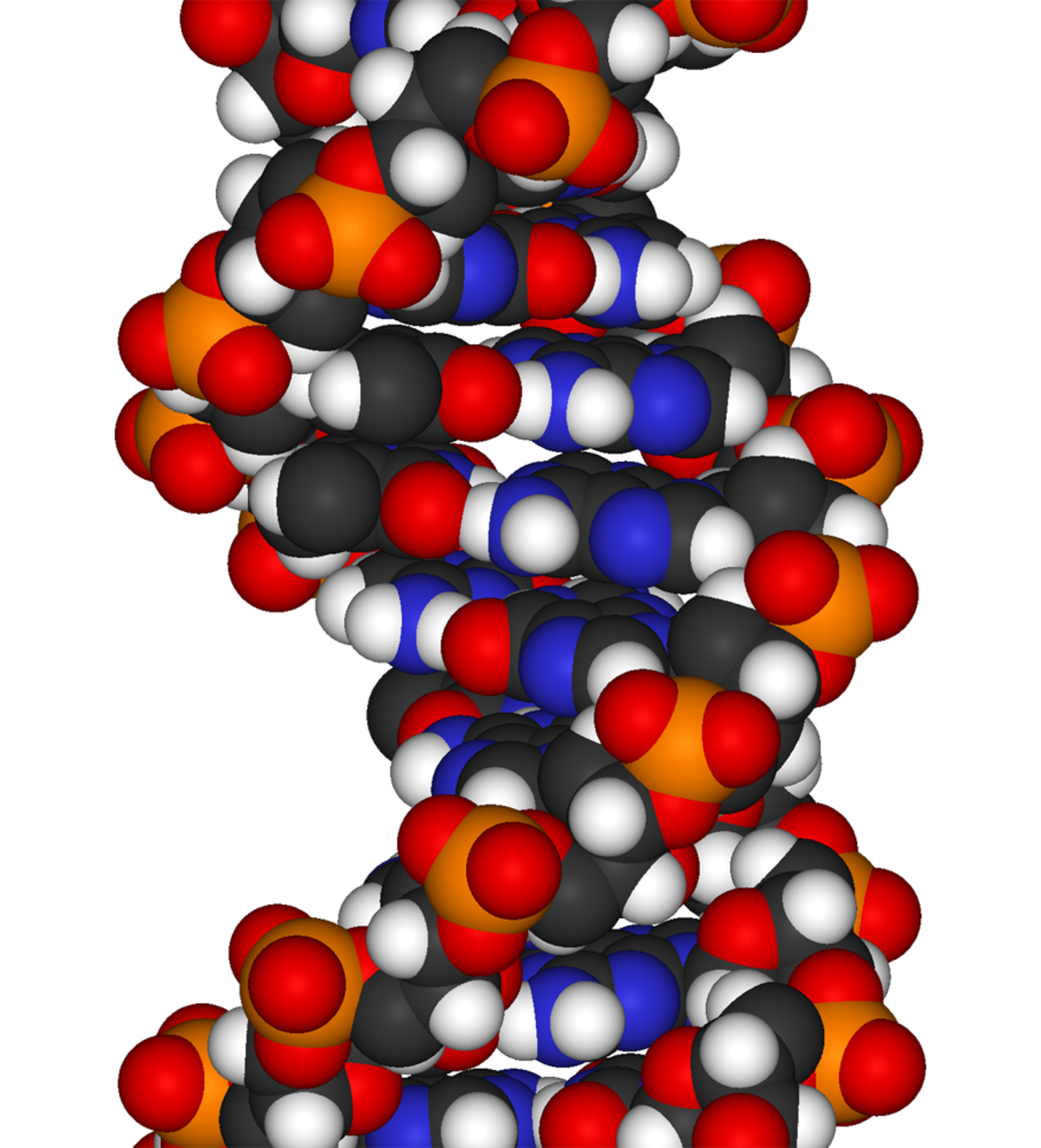
Les acides nucléiques ont été isolés initialement des noyaux des cellules eucaryotes (du latin nucleus, noyau). Ce sont des macromolécules comportant des sous-unités appelées nucléotides. On peut en distinguer deux grands types : les acides désoxyribonucléiques (ADN) et les acides ribonucléiques (ARN). L'ADN est le support universel de l'information génétique (sauf pour certains virus). Grâce à deux fonctions catalytiques cette molécule assure la transmission et l'expression de l'information qu'elle contient :
- La fonction autocatalytique : permet l'autoduplication de l'ADN et assure la transmission de l'information d'une génération à une autre.
- La fonction hétérocatalytique : gouverne la synthèse protéique. Étant donné que les enzymes sont des protéines et que toutes les synthèses et réactions dépendent d'elles, l'ADN contrôle toute l'organisation et les processus biologiques des cellules et des organismes. Ainsi, l'ADN exprime l'information qu'il comprend.
Structure
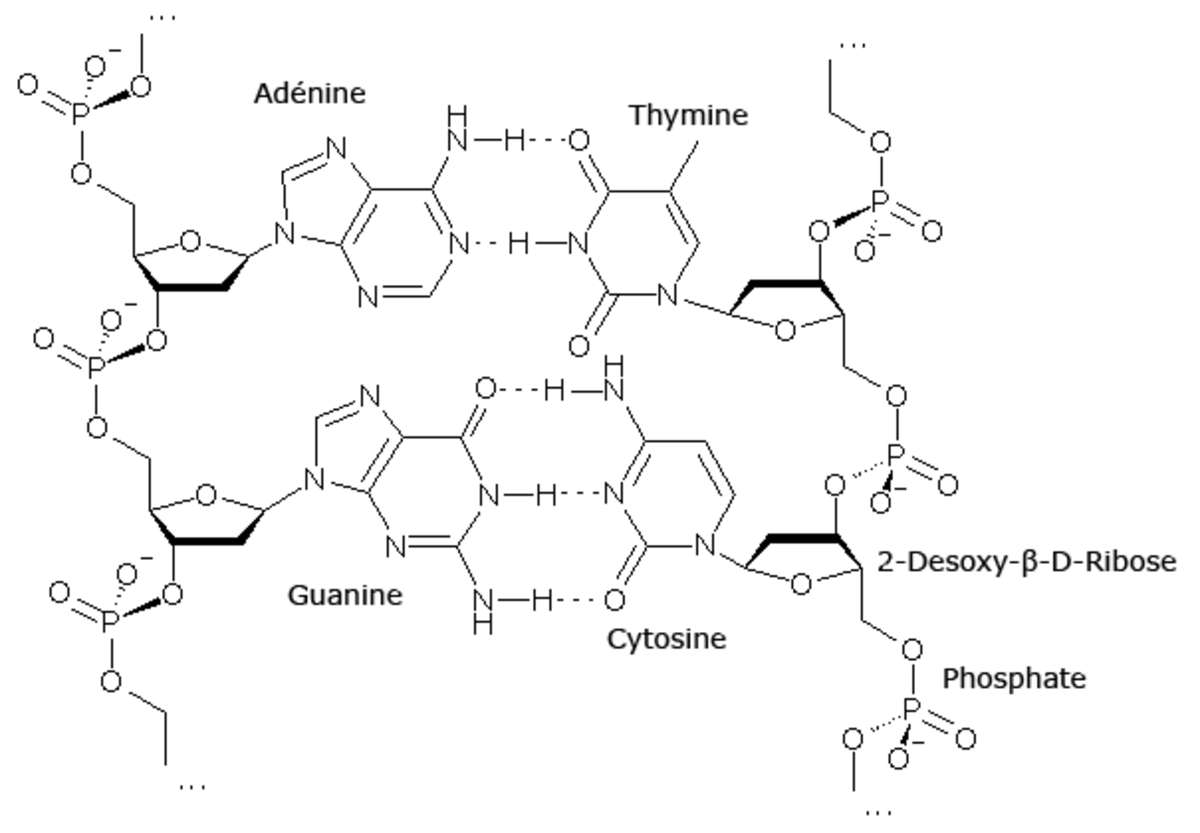
Le nucléotide, unité de base des acides nucléiques, comporte trois composants: de l'acide phosphorique, un pentose et une base azotée :
- L'acide phosphorique (H3PO4) possède 3 fonctions acides. Deux de ces fonctions sont estérifiées par deux fonctions alcools portées par les carbones 3' et 5' du pentose. La troisième fonction acide est libre. (On numérote les carbones avec des chiffres accompagnés de l’indication (') pour éviter des confusions avec les numérotations des bases).
- Le pentose (sucre en C5) : c'est le ribose, présent sous deux formes, le 2'-désoxyribose et le 2'-oxyribose, respectivement dans l'ADN et l'ARN. La liaison pentose-base est une liaison glycosidique. Elle se forme par élimination d'une molécule d'eau entre la base et l'OH semi-acétalique situé sur le carbone 1' de l'ose. L'association pentose-base est appelée nucléoside.
- Les bases azotées sont classées en bases pyrimidiques et en bases puriques. Les principales bases pyrimidiques sont : l'uracile (U), la cytosine (C) et la thymine (T). Les principales bases puriques sont : l'adénine (A) et la guanine (G). Les bases puriques et pyrimidiques présentent des formes chimiques interconvertibles que l'on appelle des formes tautomères.
Dans l'ADN bicaténaire les bases azotées des deux brins s'apparient suivant la règle de complémentarité : À apparié avec T, C apparié avec G. Cet appariement est maintenu grâce à des liaisons hydrogène et peut donc être affecté par la chaleur (dénaturation thermique). Par convention, la séquence d'un acide nucléique est orientée dans le sens de l’extrémité 5' (comportant un groupement phosphate) vers l’extrémité 3' qui possède un OH libre. Ainsi, dans l'ADN bicaténaire (double brin), les deux brins sont disposés dans deux directions opposées. Les extrémités 5' et 3' de l'un des brins correspondent aux extrémités 3' et 5' du brin parallèle opposé (anti-parallèles). Dans l’espace les deux chaînes présentent une configuration hélicoïdale. Elles s’enroulent autour d’un axe imaginaire pour constituer une double hélice à rotation droite (dans les formes A et B de l’ADN) ou plus exceptionnellement à rotation gauche (dans la forme Z de l’ADN).
Information génétique
Classiquement, on considère que le gène est une région d'un brin d'ADN dont la séquence code l'information nécessaire à la synthèse d'une protéine. Trois types d'ADN différents constituent le génome (l'ensemble des gènes d'un individu ou d'une espèce) :
- L'ADN « domestique » : représentant environ 75 % du génome, est formé de gènes présents en un seul exemplaire ou en un nombre limité de copies. Toutefois, par extension, ce type d'ADN englobe également certains gènes spécifiques dits à multicopies, comme ceux des ARN ribosomaux ou bien ceux codant les histones. Ces derniers existent sous forme de larges amas de copies (50-10 000 copies) localisés sur un ou plusieurs chromosomes.
- L'ADN « répétitif et dispersé » (minisatellites et microsatellites) : constitue 15 % du génome et est caractérisé par de courtes séquences nucléotidiques (supérieures à 100 pour les minis), répétées en tandem un très grand nombre de fois (105 - 106 fois), en de nombreuses régions du génome.
- L'ADN « satellite » : (environ 10 % du génome) est constitué de séquences hautement répétitives, essentiellement localisées dans les régions des centromères et des télomères.
Le génome humain comprend environ 3 milliards de paires de nucléotides représentant près de 30 000 gènes (en fait, dans les estimations récentes, c'est entre 20 000 et 25 000 gènes). Toutefois, il ne semble pas y avoir de relation systématique entre le nombre de paires de nucléotides par génome et le degré de complexité d'un organisme. Ainsi, certaines plantes et organismes amphibiens possèdent un génome comptant plus de 100 milliards de paires de nucléotides, soit 30 fois plus qu'un génome humain. En effet, le génome des cellules eucaryotes semble contenir un large excès d'ADN. Chez les mammifères, moins de 10 % du génome serait utile à l'expression en protéines ou à la régulation de cette expression.
| La séquence complète du gène humain HSMG03 codant l'exon 3 de la myoglobine (taille: 1,2 kb), 3 milliards de ces 4 lettres forment le génome de l'espèce humaine (Homo sapiens). |
|---|
| (d'après Weller et al., 1984. EMBO J. 3(2); 439-446) |
La taille des gènes peut varier de quelques centaines à plusieurs dizaines de milliers de nucléotides. Cependant même les plus longs gènes n'utilisent qu'une faible portion de leur séquence pour coder l'information nécessaire à l'expression en protéines. Ces régions codantes sont appelées exons et les séquences non codantes introns. D'une manière générale, plus l'organisme est complexe, plus la quantité et la taille des introns est importante. Ainsi la présence d'introns sur l'ADN d'organismes procaryotes est extrêmement rare. Certaines régions de l'ADN sont impliquées dans la régulation de l'expression des gènes. Ces séquences de régulation sont généralement localisées en amont (du côté 5') ou en aval (côté 3') d'un gène et plus rarement à l'intérieur d'introns ou d'exons.
Vitamines

Les vitamines (du latin vita, vie) sont des composés organiques essentiels à la vie, agissant à de très faibles quantités, pour le développement, l'entretien et le fonctionnement de l'organisme. Nos cellules sont incapables de les synthétiser et elles doivent être apportées par l'alimentation sous peine d'avitaminose ou de survitaminose. La vitamine B (thiamine) est la première vitamine à avoir été découverte par le japonais Suzuki Umetaro cherchant à soigner le béribéri (une maladie due au déficit en vitamine B, caractérisée par des atteintes musculaires et neurologiques). Elle fut isolée par Kazimierz Funk (biochimiste américain d'origine polonaise) en 1912. Aujourd'hui, on connaît 13 vitamines différentes pour l'homme. C'est un ensemble hétérogène du point de vue chimique et physiologique (mode d'action).
Les vitamines se divisent en deux grandes catégories : les vitamines hydrosolubles (groupes B et C) et les vitamines liposolubles (les groupes A, D, E, et K). Les vitamines hydrosolubles ne peuvent pas franchir la membrane cellulaire et elle doivent se fixer à un récepteur pour pénétrer la cellule. Elles sont facilement éliminées par les reins et la sueur, l'alimentation doit les fournir quotidiennement. Les vitamines liposolubles peuvent facilement traverser la membrane cellulaire. Leur récepteur se trouve dans la cellule, soit dans le cytosol, soit dans le noyau. Elles sont stockées dans le tissu adipeux et le foie (d'où le risque de surdosage, surtout pour la vitamine A et D). Certaines vitamines sont des cofacteurs nécessaires à l'activité d'enzymes (vitamines du groupe B), d'autres constituent une réserve de pouvoir réducteur (vitamine C, E). Les fonctions des autres vitamines restent à élucider.