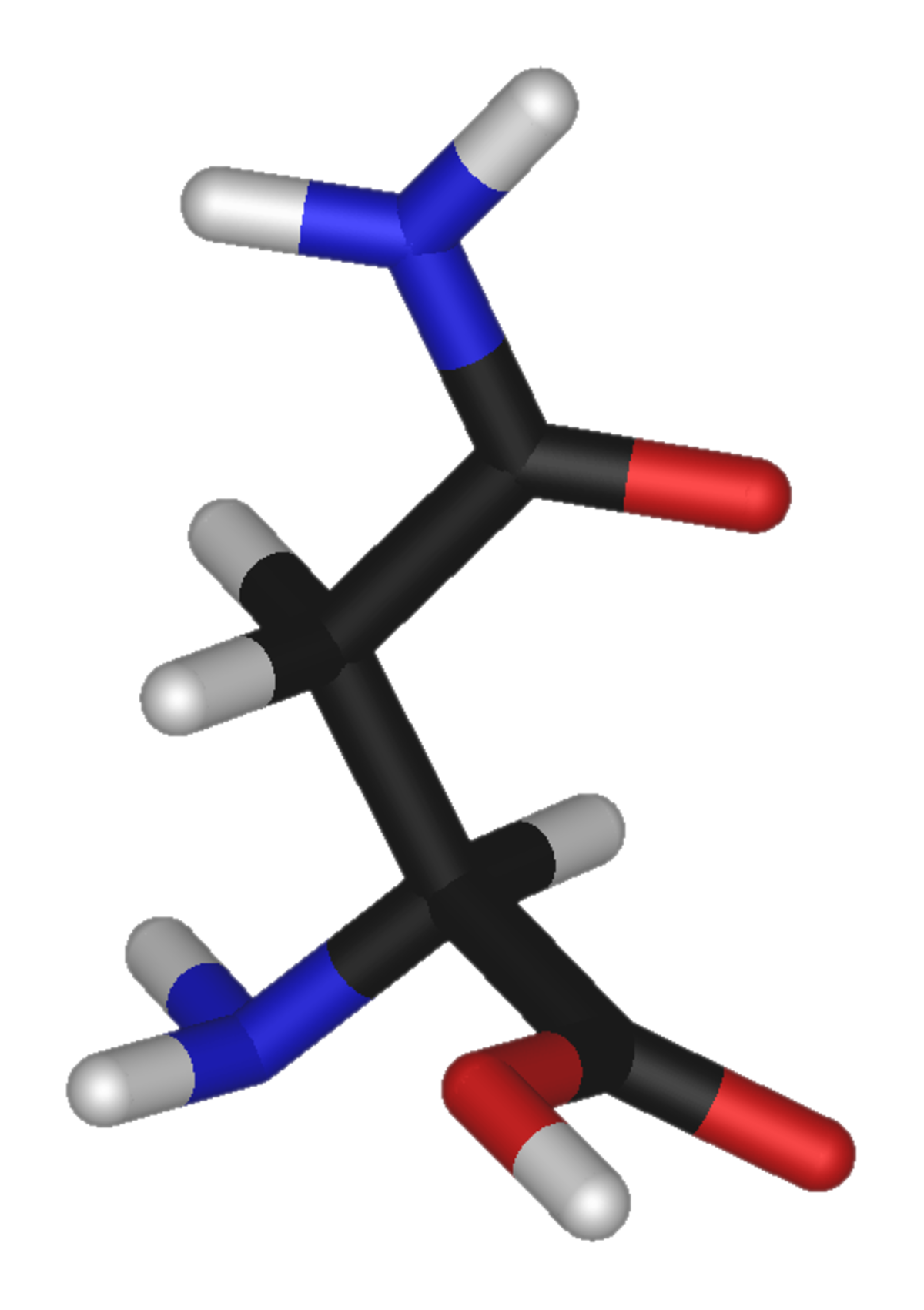
Asparagine - Définition
Source: Wikipédia sous licence CC-BY-SA 3.0.
La liste des auteurs de cet article est disponible ici.
La liste des auteurs de cet article est disponible ici.
Introduction
| Asparagine | |
|---|---|
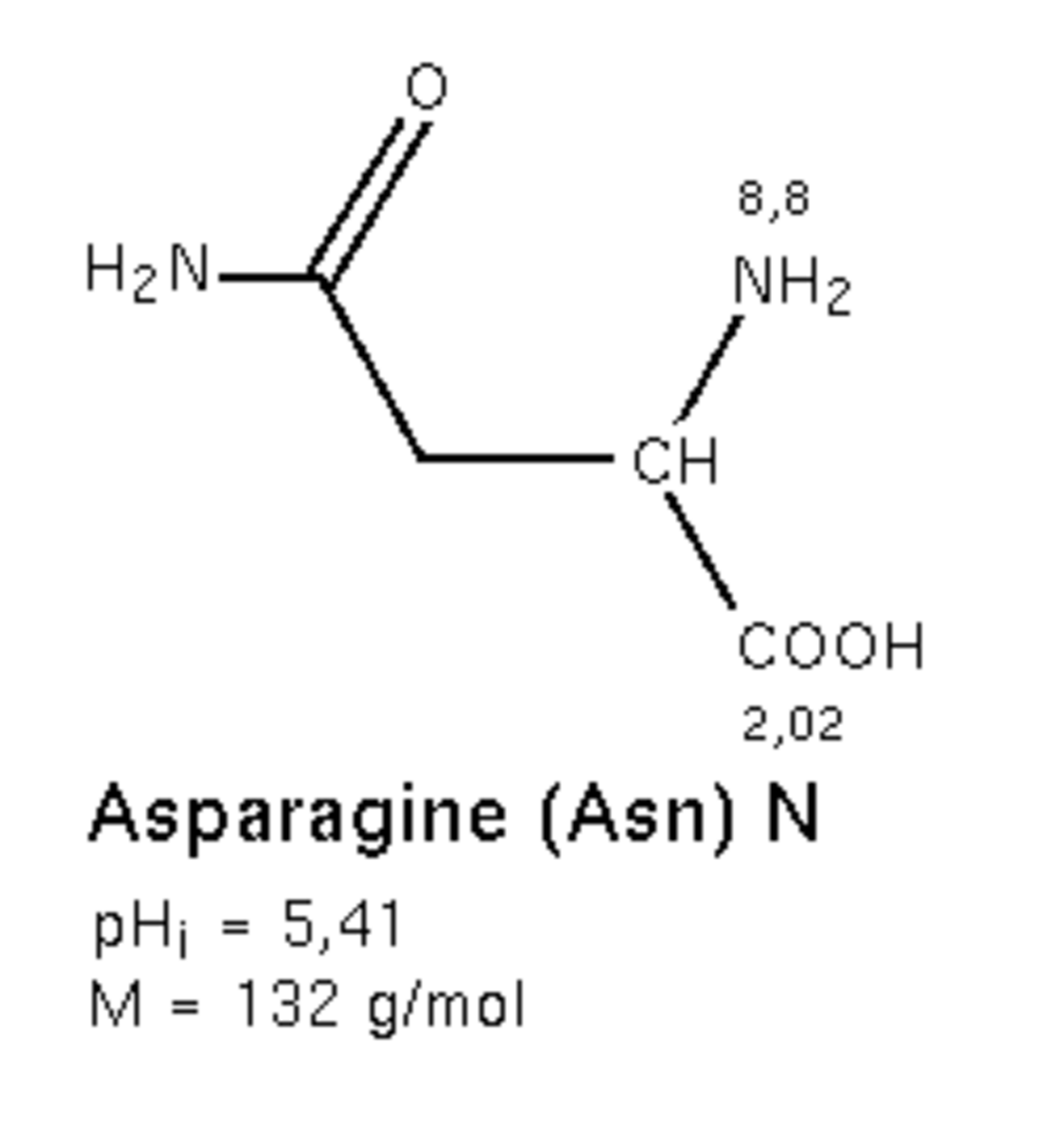
| |
| Général | |
| Nom IUPAC | |
| Synonymes | N, Asn, acide (2S)-2-amino- 3-carbamoyl-propanoïque |
| No CAS | (racémique) (D) ou R(+) (L) ou S(–) |
| No EINECS | (L) |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule brute | C4H8N2O3 |
| Masse molaire | 132,1179 ± 0,0051 g·mol-1 |
| pKa | 2,16 8,73 |
| Propriétés physiques | |
| Masse volumique | 1 g·cm-3 |
| Propriétés biochimiques | |
| Codons | AAU, AAC |
| pH isoélectrique | 5,41 |
| Acide aminé essentiel | Non |
| Occurrence dans les protéines | 4,3 % |
| Précautions | |
| | |
| Produit non contrôlé | |
| | |
L'asparagine (ou acide asparagine-amino-succinique) est un acide α-aminé polaire non chargé et hydrophile, dérivé de l'acide aspartique. L'asparagine est l'amide (au niveau du radical) de l'acide aspartique.
L'asparagine est un des vingt acides aminés naturels les plus communs sur terre. Elle est considérée comme un acide aminé non-essentiel (c.a.d. ne nécessitant pas d'apport extérieur, car le corps peut la synthétiser). Dans les protéines, l'asparagine participe à la formation de liaisons hydrogènes par son groupe amide.
Anecdotes
- L'asparagine fut le premier acide aminé découvert en 1806 par Louis-Nicolas Vauquelin qui étudiait alors les asperges, d'où son nom.
- On associe souvent l'odeur caractéristique des urines après avoir mangé des asperges à l'asparagine, mais certains scientifiques sont en désaccord et impliquent d'autres substances comme les méthanethiols.
Fonctions structurelles
Sur l'asparagine se branchent des oligosacharides lors de la N-glycosylation