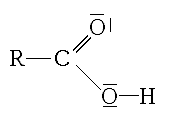
Acide carboxylique - Définition
La liste des auteurs de cet article est disponible ici.
Dérivés
Les acides carboxyliques comptent de nombreux dérivés :
- les chlorures d'acyle
- les anhydrides alcanoïques
- les esters
- les amides
- les nitriles
En termes de groupe partant (nucléofuge) l'ordre de facilité est:
Cl- (chlorure d'acyle), RCOO- (anhydride), RO- (ester), -NH2 et -NR1R2 (amides).
Réduction
- Aldéhyde
- alcool primaire
Oxydation
- dioxyde de carbone (CO2)
Réactivité
Comme le montre, entre autres, les différentes formules mésomères de l'acide carboxylique:
- Les atomes d'oxygène sont des sites nucléophiles ainsi que des bases de Lewis
- Le carbone central est électrophile
- l'atome d'hydrogène électrophile et acide.
Synthèse
Synthèse par oxydation
- des alcools ou des aldéhydes
Les acides carboxyliques peuvent être obtenus par oxydation des aldéhydes, donc en fait d'une double oxydation des alcools primaires.
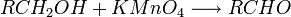
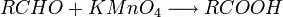
- des alcènes
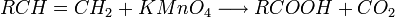
ex : Synthèse de l'Acide acétique par oxydation du propène
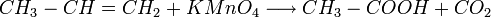
Synthèse à partir d'un dérivé d'acide
Il s'agit simplement des hydrolyses des différents dérivés d'acides
- ester
- hydrolyse en milieu acide : rétroestérification.
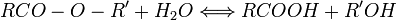
-
- hydrolyse en milieu basique : saponification de l' ester.
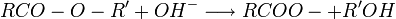
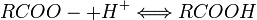
- hydrolyse en milieu basique : saponification de l' ester.
- nitrile
Synthèse par réaction d'un organomagnésien sur le dioxyde de carbone
Réaction
Conditions
La synthèse a lieu à basse température (-40 °C). Le dioxyde de carbone est alors sous forme solide, dite carboglace. Il est mis en excès. après réaction, on effectue une hydrolyse en milieu acide pour obtenir l'acide carboxylique
Mécanisme
- Première étape : addition de l'organomagnésien sur CO2
- Deuxième étape : hydrolyse en milieu acide
Synthèse malonique
La synthèse malonique est un ensemble de réactions permettant de synthétiser de nombreux acides carboxyliques primaires ou secondaires à partir du malonate de diéthyle.
Elle est composée:
- d'une réaction acide-base entre le malonate de diéthyle et de l'éthanoate (de sodium, de potassium, etc.);
- d'une substitution nucléophile, ou l'on insère le groupe (primaire ou secondaire) voulu pour l'acide carboxylique final:
- d'une double saponification des deux fonctions ester du malonate de diéthyle subsititué, suivie d'une acidification du milieu;
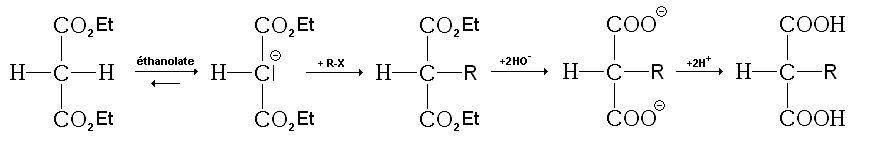
- d'une décarboxylation (dégagement de dioxyde de carbone par chauffage)
- d'un réarrangement du produit final en acide carboxylique par tautomérie.
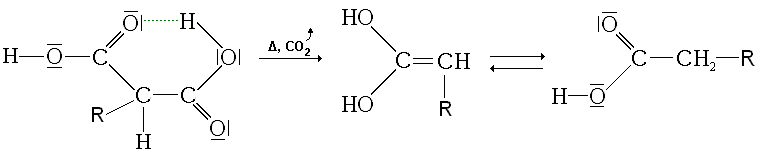
Cette synthèse est d'autant plus intéressante qu'a priori, elle permet de synthétiser n'importe quel acide carboxylique, puisque, à part un groupe tertiaire, il semble qu'on puisse mettre ce qu'on veut à la place de R.