Acide aspartique - Définition
|
||||
|---|---|---|---|---|
|
||||
| Nom IUPAC | acide (2S)-2-aminobutanedioïque | |||
| Abréviations | D (Asp) | |||
| Formule brute | C4H7O4N | |||
| Masse molaire | 133,10 g/mol | |||
| N° CAS | 56-84-8 | |||
| Codons | GAU, GAC | |||
| Point de fusion | 270–271 °C | |||
| pH isoélectrique | 2,85 | |||
| pKa | 2,0 10,0 3,9 |
|||
| Pouvoir rotatoire | +5,0° .dm-1.g-1.cm3 ° | |||
| Rayon de van der Waals | 91 Å | |||
| Aspect | ? | |||
| Masse volumique | 1,66 g/cm3 | |||
| Solubilité dans l'eau | 4 g/L (20 °C) | |||
| Solubilité dans l'éthanol | ||||
| Essentiel | Non | |||
| Occurrence dans les protéines | ? | |||
|
|
||||
|
|
||||
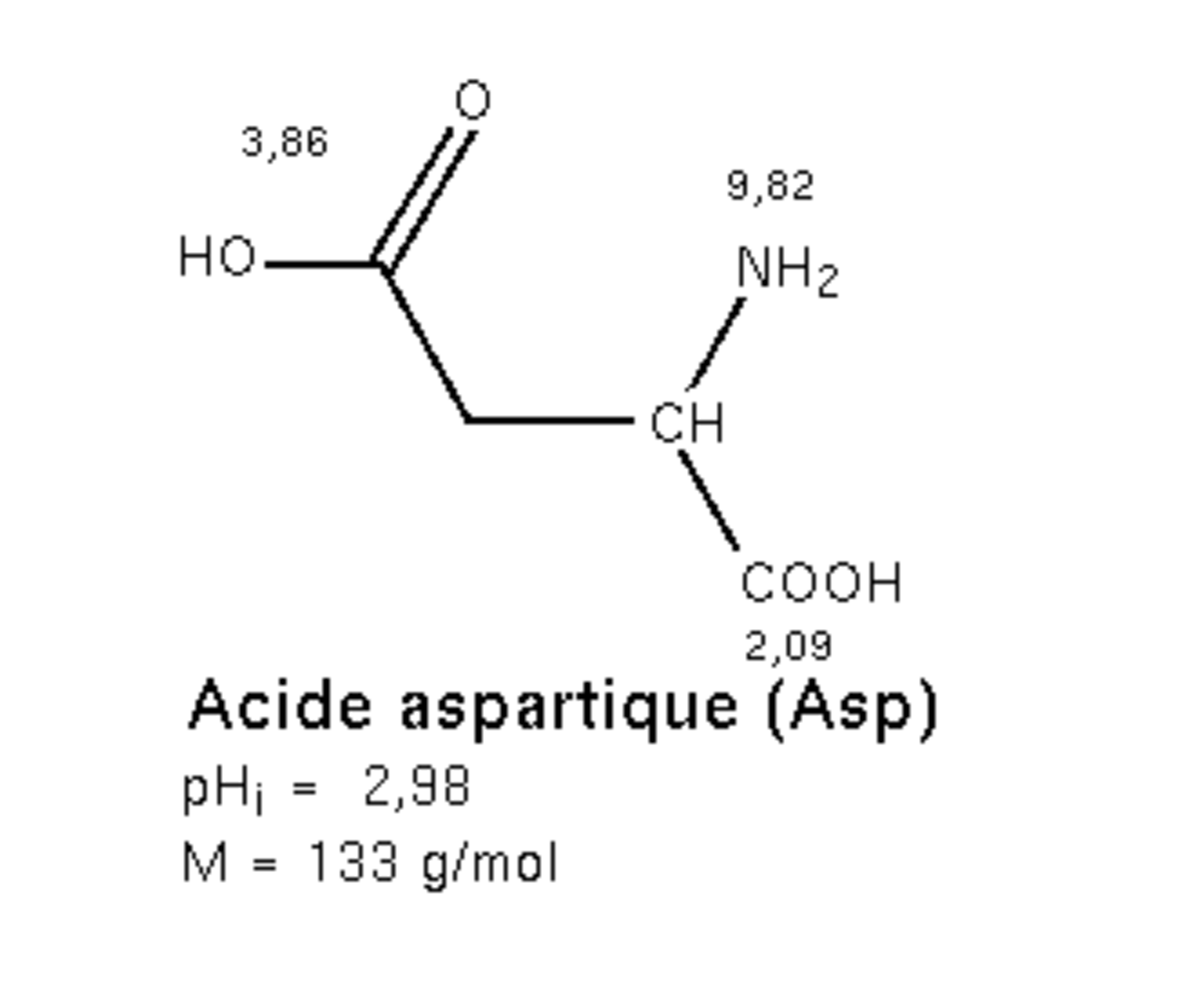
L’acide aspartique (dont l'anion s'appelle aspartate) est l'un des 20 acides-α-aminés constituant les protéines. Il s'agit de l'acide carboxylique proche de l'asparagine. C'est un acide dicarboxylique, polaire. Chez les mammifères, il est non-essentiel, et peut servir de neurotransmetteur excitant dans le cerveau sous sa forme méthylée (récepteur NMDA, N-méthyl D-aspartate, récepteur au glutamate). C'est un métabolite du cycle de l'urée, et il participe à la gluconéogénèse.
L’acide aspartique a un point isoélectrique de 2,85 ce qui en fait le plus acide des acides aminés.
Acide aspartique et aspartame
L'acide aspartique représente 40 % des produits de métabolisation de l’aspartame (

Le Dr. Russell L. Blaylock, professeur en neurochirurgie à l'université de médecine du Mississippi, a récemment publié un ouvrage détaillant les dommages causés par l'ingestion excessive d'acide aspartique issu de l'aspartame. Il fait mention de près de 500 références scientifiques afin de démontrer comment un excès d'acides aminés libres excitateurs tel que l'acide aspartique dans notre alimentation sont causes de sérieux désordres neurologiques chroniques.
Réalité sur l’acide aspartique
L'acide aspartique n'est dangereux que lorsque son taux dans le plasma dépasse 100 µmol/dl. Or, même à la dose extrême de 200 mg/kg de poids corporel, le niveau d'acide aspartique dans le sang n'approche pas le seuil réputé toxique. De plus, les aliments édulcorés ne constituent pas les sources principales en acide aspartique. Par conséquent, cette toxicité ne se rencontrerait pas chez les humains suite à la consommation alimentaire habituelle d’aspartame, d'après le professeur John Fernstrom de l'université de Pittsburg.