Pile à combustible - Définition
Une pile à combustible est une pile où la fabrication de l'électricité se fait grâce à l'oxydation sur une électrode d'un combustible réducteur (par exemple l'hydrogène) couplée à la réduction sur l'autre électrode d'un oxydant, tel que l'oxygène de l'air.
Historique
1839 Découverte de l' effet pile à combustible par le suisse Christian Schönbein
1839-1842 Réalisation du premier modèle de laboratoire de pile à combustible par William R. Grove
1932 Reprise des études au sujet de la pile à combustible par Francis T. Bacon, qui réalise un premier prototype de 1kW en 1953, puis 5kW en 1959. Ce prototype servira de modèle pour les futures piles à combustible utilisées lors des missions spatiales Apollo.
Le très long laps de temps (plus d'un siècle) qui s'est écoulé entre la réalisation du premier modèle de pile à combustible et les premières utilisations s'explique par le très fort développement qu'ont connu les autres types de générateurs d'énergie électrique et par le fait que le coût des matériaux utilisés dans la pile à combustible reste encore actuellement élevé.
Généralités
Une pile à combustible est une pile où la fabrication de l'électricité se fait grâce à l'oxydation sur une électrode d'un combustible réducteur (par exemple l'hydrogène) couplée à la réduction sur l'autre électrode d'un oxydant, tel que l'oxygène de l'air. La réaction d'oxydation de l'hydrogène est accélérée par un catalyseur qui est généralement du platine. Si d'autres combinaisons sont possibles, la pile la plus couramment étudiée et utilisée est la pile hydrogène-oxygène ou hydrogène-air.
Pile à combustible à l'hydrogène
Le fonctionnement d'une pile hydrogène-oxygène est particulièrement propre puisqu'il ne produit que de l'eau et consomme uniquement des gaz. Mais jusqu'en 2006, la fabrication de ces piles est très coûteuse, notamment à cause de la quantité non négligeable de platine nécessaire.
Une des difficultés majeures réside dans la synthèse et l'approvisionnement en hydrogène. Sur Terre, l'hydrogène n'existe en grande quantité que combiné à l'oxygène (H2O), au soufre (H2S) et au carbone (combustibles fossiles de types gaz ou pétroles). La production d'hydrogène nécessite donc soit de consommer des combustibles fossiles, soit de disposer d'énormes quantités d'énergie à faible coût, pour l'obtenir à partir de la décomposition de l'eau, par voie thermique ou électrochimique.
Ensuite, l'hydrogène peut être comprimé dans des bouteilles à gaz (pression en général de 350 ou 700 bars), ou liquéfié ou combiné chimiquement sous forme de méthanol ou de méthane qui seront ensuite transformés pour libérer de l'hydrogène. Les rendements énergétiques cumulés des synthèses du dihydrogène, de compression ou liquéfaction, sont généralement assez faibles. L'hydrogène n'est donc pas une source d'énergie primaire, c'est un simple vecteur d'énergie difficile à produire et à stocker.
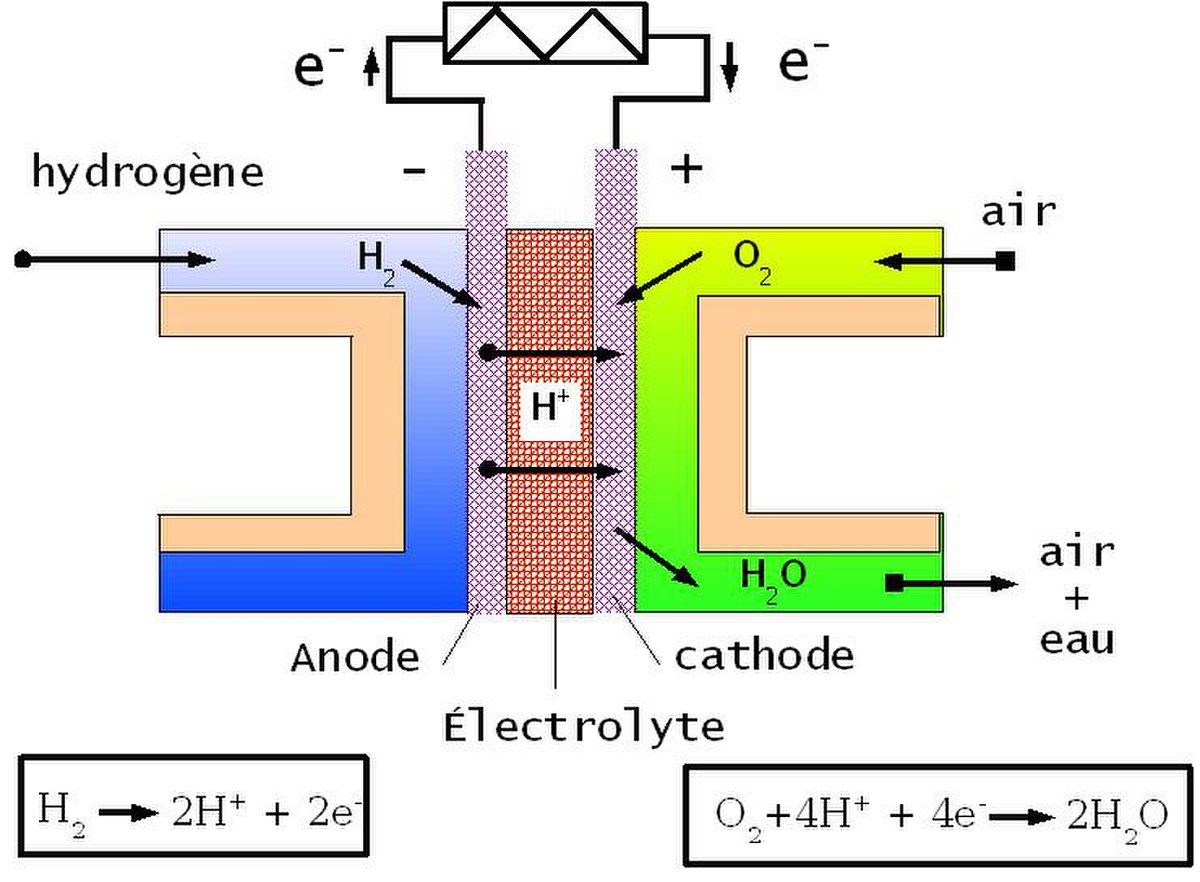
Le principe de fonctionnement
La pile à combustible fonctionne à l'inverse de l'électrolyse de l'eau. Elle transforme l'énergie chimique en énergie électrique directement. C'est un générateur.
- Elle est semblable à une pile ordinaire. Elle possède une cathode et une anode séparées par un électrolyte qui assure entre autres le passage du courant par transfert ionique des charges.
- Comme une pile classique, elle consomme son oxydant (ici l'oxygène O2) et son réducteur (ici l'hydrogène H2). Elle continue de fonctionner tant qu'elle est approvisionnée en hydrogène et oxygène. Le réducteur peut être aussi du méthanol ou du gaz naturel.
- À l'anode, a lieu la réaction suivante : H2 → 2H+ + 2e–
- Il y a donc production de 2 électrons par molécule de dihydrogène.
- L'ion H+ passe de l'anode à la cathode et provoque un courant électrique par transfert des électrons dans le circuit électrique.
- À la cathode, les ions H+ sont consommés suivant la réaction : O2 + 4H+ + 4e– → 2H2O
La tension théorique produite est de 1.23 Volt.
- Les réactions sont rendues possibles par la présence d'un catalyseur de dissociation de la molécule d'hydrogène qui peut être une fine couche de platine divisé sur un support poreux qui constitue l'électrode à hydrogène.
Pile à combustible au méthanol
Il existe deux types de piles à combustible au méthanol :
- Les piles RMFC (Reformed Methanol Fuel Cell) : dans ces piles, le méthanol est reformé pour produire l'hydrogène qui alimentera la pile.
- Les piles DMFC (Direct Methanol Fuel Cell) : dans ces piles, le méthanol est directement oxydé dans le cœur de la pile et ne nécessite pas d'être reformé.
Tableau récapitulatif des différentes technologies de piles à combustible
| Description | Électrolyte | Ions mis en œuvre | Gaz à l'anode | Gaz à la cathode | Puissance | Température de fonctionnement | Rendement électrique | Maturité | Domaine |
|---|---|---|---|---|---|---|---|---|---|
| AFC – Pile à combustible alcaline | Hydroxyde de potassium | OH– | dihydrogène | dioxygène | 10 à 100 kW | 60°C – 90°C | Stack : 60–70 % Système : 62 % | Commercialisé/ Développement | Portable, transport |
| DBFC – Pile à combustible à hydrure de bore direct | Membrane protonique
Membrane anionique |
H+
OH– |
NaBH4 liquide | oxygène | 250mW/cm² | 20°C – 80°C | 50% monocellule | Développement | portable <20W |
| PEMFC – Pile à combustible à membrane d'échange de protons | Membrane polymère | H+ | dihydrogène | dioxygène | 0,1 à 500 kW | 60–100°C | Stack : 50–70 % Système : 30–50 % | Commercialisé/ Développement | portable, transport, stationnaire |
| DMFC – Pile à combustible à méthanol direct | Membrane polymère | H+ | méthanol | dioxygène | mW à 100 kW | 90–120°C | Stack : 20–30 % | Commercialisé/ Développement | transport, stationnaire |
| DEFC – Pile à combustible à éthanol direct | 90–120°C | Développement | |||||||
| FAFC – Pile à combustible à acide formique | 90–120°C | Développement | |||||||
| PAFC – Pile à combustible à acide phosphorique | Acide phosphorique | H+ | dihydrogène | dioxygène | jusqu'à 10 MW | environ 200°C | Stack : 55 % Système : 40 % | Développement | transport, stationnaire |
| MCFC – Pile à combustible à carbonate fondu | Carbonate de métaux alcalins | CO32– | dihydrogène, Méthane, Gaz de synthèse | dioxygène | jusqu'à 100 MW | environ 650°C | Stack : 55 % Système : 47 % | Développement/ Mise sur le marché | stationnaire |
| PCFC – Pile à combustible à céramique protonante | 700°C | Développement | |||||||
| SOFC – Pile à combustible à oxyde solide | Céramique | O2– | dihydrogène, Méthane, Gaz de synthèse | dioxygène | jusqu'à 100 MW | 800–1050°C | Stack : 60–65 % Système : 55–60 % | Développement | stationnaire |
Applications et perspectives
Grâce aux progrès incessants de cette technologie, dont les premiers développements dans le domaine spatial remontent aux années 1960, et à la baisse des prix, son utilisation croît dans de nouveaux domaines. Notamment pour alimenter des prototypes d'ordinateurs portables, de téléphones portables ou d'appareils photo ou encore de véhicules propres.
Cependant, la viabilité industrielle à grande échelle de tels systèmes se heurte au faible rendement énergétique global de l'ensemble des opérations. En effet, chaque étape (synthèse de l'hydrogène, séchage du gaz, stockage, vaporisation, rendement des réactions électrochimiques de la pile, circulation des fluides, régulation thermique, maintenance, récupération du platine, etc.) écorne un rendement global encore très décevant. Il suppose donc la disponibilité d'une source d'énergie primaire économique et inépuisable à l'échelle humaine.
D'autres voies de stockage et de transport de l'hydrogène peuvent aussi être envisagées pour réduire les pertes, comme par exemple, le conditionnement solide et stable de l'hydrogène sous forme de pastilles aminées.
L'utilisation de la pile à combustible en cogénération, permettant de valoriser la production thermique de la pile, est considérée d'un point de vue environnemental et technique comme avantageuse mais demeure encore trop chère pour une utilisation courante.
Programmes de recherche ou de développement
Par zones géographiques
Les USA développent de nombreux projets soutenus par le gouvernement, parfois présentés comme une des solutions majeures contre le réchauffement climatique.
Au Canada, l'Institut d'Innovation en Piles à Combustible du Conseil National de Recherches du Canada (IIPC-CNRC), a été créé en septembre 2006 sur 6500 m², en Colombie britannique (UBC), dans la grappe technologique de la région de Vancouver, pilote dans ce domaine.
Il vise à développer l'industrie de l'hydrogène et des piles à combustible au Canada. C’est une plate-forme de démonstration autant que de recherche, qui abrite aussi le Programme de Vancouver sur les véhicules à piles à combustible, ainsi que le projet d’autoroute de l'hydrogène de la Colombie britannique, épaulés par des labos consacrés à l'alimentation en hydrogène et aux technologies de piles à combustible intégrées. Le site dispose de pompes géothermiques et de moyens photovoltaïques de production d'hydrogène.
En France, l’ADEME, EDF et le CEA ont installé un RESEAU "PILE A COMBUSTIBLE le 25 juin 1999 piloté par Catherine Ronge, directrice R&D d'Air liquide et Roger Ballay, directeur adjoint de la recherche à EDF, co-animé par l'ADEME et le Commissariat à l'Energie Atomique (CEA) avec pour mission d’accélérer les recherches sur la pile à combustible en identifiant les verrous technologiques, en animer la communauté scientifique autour d’un pôle d'expertise susceptible de valoriser et diffuser les avancées de la recherche, de développer les partenariats public-privé une réflexion prospective sur le développement de ces technologies.
Automobile
- Daimler :
- Ford :
-
- Focus FCV
- General Motors :
-
- Hydrogen 3 présenté en mai 2004.
- Sequel voiture. La pile à hydrogène de 73 kW est alimentée par trois bouteilles à gaz bobinées composite de dihydrogène de 700 bars (2005).
- Chevy Volt: concept présenté en janvier 2007 au salon automobile de Detroit (USA).
- Michelin :
-
- prototype de voiture Hy-light fonctionnant avec une pile à hydrogène (présentation en mars 2005). La pile est alimentée par du dihydrogène provenant de trois bouteilles haute pression bobinées composite.
- PSA :
-
- Projet GENEPAC (2002-2006) mené en collaboration avec le CÉA. Pile hydrogène de type PEMFC de 80 kW.
- Toyota :
-
- Voiture cinq places FCHV-4 et bus FCHV-US1. Ces programmes ont été présentés pour la première fois en 2001. Ils comportent une pile à hydrogène de 90 kW.
- Suzuki (en collaboration avec General Motors) :
-
- Prototype de voiture Mr Wagon FCW'. La pile à hydrogène est alimentée par du dihydrogène contenu dans des réservoirs à 700 bars.
- Hyundai :
- Honda :
-
- Honda FCX
- Hummer :
-
- Hummer O2
-
- Le modèle expérimental 207 CC
- BMW:
-
- BMW Hydrogen 7
- N'utilise pas de pile à combustible. Il s'agit d'un moteur à combustion classique utilisant de l'hydrogène comme combustible.
Autres domaines
- Axane (Air liquide) :
-
- Evopac, système d'alimentation autonome alimenté par du dihydrogène.
- Système de refroidissement par évaporation inspiré des plantes vertes pour les piles à combustible des ordinateurs portables de demain.