Le rajeunissement cellulaire enfin possible grâce à cette protéine 🧬
Publié par Cédric,
Auteur de l'article: Cédric DEPOND
Source: Cellular Signalling
Autres langues: EN, DE, ES, PT
Auteur de l'article: Cédric DEPOND
Source: Cellular Signalling
Autres langues: EN, DE, ES, PT
Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)

Des chercheurs de l'Université d'Osaka, au Japon, ont peut-être percé le secret du vieillissement cellulaire. Leurs travaux, publiés dans la revue Cellular Signaling, révèlent le rôle clé d'une protéine, AP2A1, dans le processus de sénescence. Cette découverte ouvre la voie à des traitements qui pourraient inverser les effets du temps sur nos cellules, et par conséquent, sur notre organisme tout entier.
AP2A1: le chef d'orchestre du vieillissement cellulaire ?
Avec l'âge, nos cellules subissent des transformations. Certaines deviennent sénescentes, c'est-à-dire qu'elles cessent de se diviser et perdent leurs fonctions. Ces cellules, plus grandes que les cellules jeunes, présentent des modifications au niveau de leurs "fibres de stress", des structures qui leur permettent de se mouvoir et d'interagir avec leur environnement. Les scientifiques cherchent à comprendre comment ces cellules sénescentes parviennent à conserver leur taille imposante.
L'équipe de l'Université d'Osaka s'est intéressée à la protéine AP2A1. Cette protéine, présente en plus grande quantité dans les fibres de stress des cellules sénescentes, pourrait jouer un rôle clé dans le vieillissement cellulaire. Pour vérifier cette hypothèse, les chercheurs ont modulé l'expression de la protéine AP2A1 dans des cellules jeunes et âgées.
Les résultats de ces expériences ont été surprenants. La suppression de l'expression d'AP2A1 dans les cellules âgées a entraîné une inversion de la sénescence et une revitalisation cellulaire. Inversement, l'augmentation de l'expression d'AP2A1 dans les cellules jeunes a accéléré le processus de sénescence. Ces observations suggèrent qu'AP2A1 agit comme un interrupteur entre les états "jeune" et "vieux" des cellules.
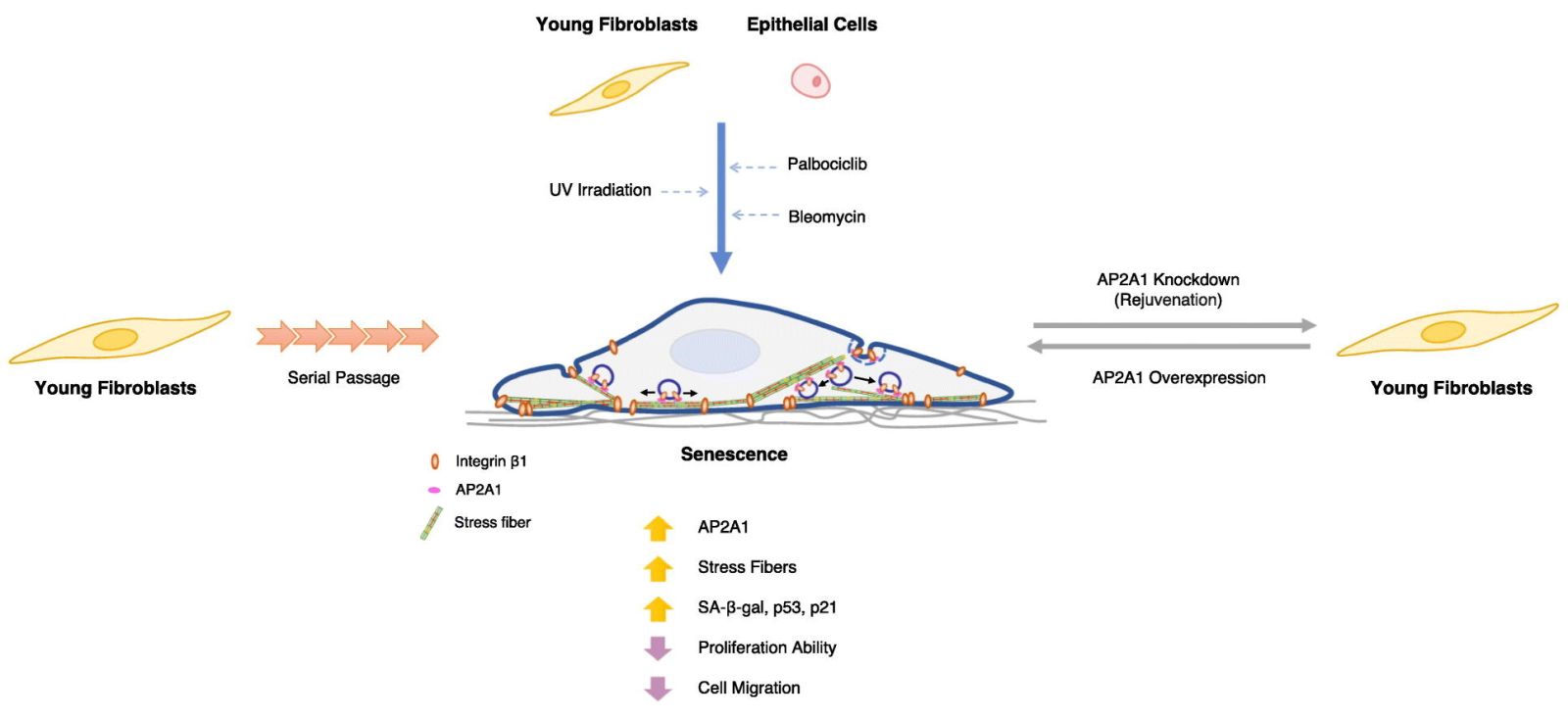
L'interaction avec l'intégrine β1
Les chercheurs ont également découvert qu'AP2A1 interagit étroitement avec une autre protéine, l'intégrine β1. Cette dernière permet aux cellules de s'ancrer à la matrice extracellulaire, un réseau de protéines qui les entoure. AP2A1 et l'intégrine β1 se déplacent ensemble le long des fibres de stress. L'intégrine β1 renforce l'adhésion des cellules au substrat, ce qui pourrait expliquer la taille accrue des cellules sénescentes.
La forte corrélation entre l'expression d'AP2A1 et la sénescence cellulaire en fait un candidat prometteur comme marqueur du vieillissement cellulaire. De plus, le rôle actif d'AP2A1 dans le processus de vieillissement ouvre la voie à de nouvelles stratégies thérapeutiques pour lutter contre les maladies liées à l'âge.
Pour aller plus loin: Qu'est-ce que la sénescence cellulaire ?
La sénescence cellulaire est un état dans lequel une cellule cesse de se diviser, mais sans pour autant mourir. Elle se distingue de l'apoptose (la mort cellulaire programmée) et de la nécrose (la mort cellulaire accidentelle). Les cellules sénescentes sont souvent plus grandes que les cellules jeunes et présentent des modifications morphologiques, notamment au niveau de leur cytosquelette et de leurs organites. Elles peuvent rester métaboliquement actives et sécréter diverses molécules, telles que des facteurs inflammatoires, des facteurs de croissance et des enzymes de dégradation de la matrice extracellulaire.
La sénescence cellulaire peut être déclenchée par différents facteurs, tels que des dommages à l'ADN, le raccourcissement des télomères (les extrémités des chromosomes), le stress oxydatif, l'activation d'oncogènes ou encore des signaux extracellulaires. Elle est considérée comme un mécanisme de protection contre la prolifération cellulaire incontrôlée, notamment en cas de dommages à l'ADN qui pourraient conduire à la formation de cellules cancéreuses. Cependant, l'accumulation de cellules sénescentes dans les tissus peut avoir des effets néfastes sur l'organisme, en contribuant au vieillissement et au développement de maladies liées à l'âge.
Les cellules sénescentes peuvent avoir des effets variables sur les tissus environnants. Dans certains cas, elles peuvent favoriser la réparation tissulaire et l'homéostasie. Dans d'autres cas, elles peuvent contribuer à l'inflammation chronique, à la fibrose (la formation excessive de tissu conjonctif) et à la perte de fonction des organes. L'équilibre entre les effets bénéfiques et néfastes de la sénescence cellulaire dépend du contexte et du type de cellules concernées. La recherche sur la sénescence cellulaire est en plein essor, avec pour objectif de mieux comprendre son rôle dans le vieillissement et les maladies, et de développer de nouvelles stratégies thérapeutiques pour moduler ses effets.