Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
Mêmes atomes, mais formes différentes, certains produits avec une formule chimique identique présentent des propriétés parfois divergentes: une molécule pouvant être recherchée et l'autre nocive. Grâce à un système catalytique optimal, des scientifiques de l'Institut de Chimie des Substances Naturelles (ICSN, CNRS) favorisent la formation d'une de ces deux molécules, tout en réduisant les quantités de réactifs coûteux. Ces travaux sont publiés dans le Journal of the American Chemical Society.
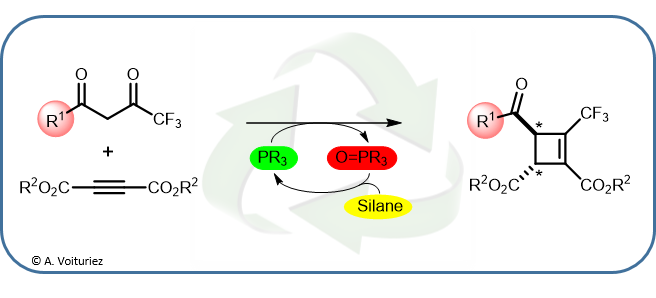
© Arnaud Voituriez
Les phosphines trivalentes (PR3) servent de réactifs dans de nombreuses transformations chimiques où la phosphine est généralement oxydée (O=PR3). Très efficaces, ces réactions génèrent cependant une quantité importante de déchets, ce qui complique la purification. Afin de limiter les quantités utilisées de ces phosphines, souvent dispendieuses, des chercheurs de l'Institut de Chimie des Substances Naturelles (ICSN, CNRS) emploient un agent réducteur qui retransforme les oxydes de phosphine en phosphine, au fur et à mesure de leur formation.
Cette méthode a été utilisée pour la synthèse efficace de différents cyclobutènes chiraux, des molécules très prisées en synthèse organique. Une molécule non superposable à son image dans un miroir est dite "chirale", et les deux molécules images l'une de l'autre sont appelées "énantiomères". Cette différence a priori minime modifie en réalité en profondeur les propriétés des molécules, qui peuvent même être opposées. Or le procédé des chercheurs de l'ICSN est justement sélectif: il produit majoritairement un seul des deux énantiomères. Cette méthode est d'autant plus avantageuse qu'elle utilise une très faible quantité de phosphine chirale extrêmement coûteuse. Ces travaux constituent une preuve de concept pour une production plus écologique et plus économique de molécules chirales, en particulier dans les domaines pharmaceutiques et de l'agrochimie.
Références:
Lorton C., Castanheiro T. et Voituriez A.
Catalytic and Asymmetric Process via PIII/PV═O Redox Cycling: Access to (Trifluoromethyl)cyclobutenes via a Michael Addition/Wittig Olefination Reaction.
J. Am. Chem. Soc. - Juin 2019
DOI: 10.1021/jacs.9b02539
Contacts checheurs:
- Arnaud Voituriez - Chercheur (ICSN UPR2301) - arnaud.voituriez at cnrs.fr
- Stéphanie Younès - Responsable Communication - inc.communication at cnrs.fr
- Christophe Cartier dit Moulin - INC & Institut parisien de chimie moléculaire - inc.communication at cnrs.fr
- Sophie Félix - Chargée de communication - inc.communication at cnrs.fr
Populaires