Restez toujours informé: suivez-nous sur Google Actualités (icone ☆)
Le bicarbonate de soude est un composé aux multiples usages aussi bien en cuisine que pour le nettoyage. Pour les chimistes, il pourrait en fait être responsable de la charge négative aux interfaces entre l'eau et des composés hydrophobes. Ces travaux impliquant des chercheurs du laboratoire Ingénierie des matériaux polymères (CNRS/Université Jean Monnet/INSA Lyon/Université Claude Bernard), de l'Institut Charles Gerhardt Montpellier (CNRS/Université de Montpellier/ENSC Montpellier), du laboratoire Charles Coulomb (CNRS/Université de Montpellier) et de l'Institut Charles Sadron (CNRS) ont fait l'objet de deux publications successives dans la revue Journal of Physical Chemistry Letters.
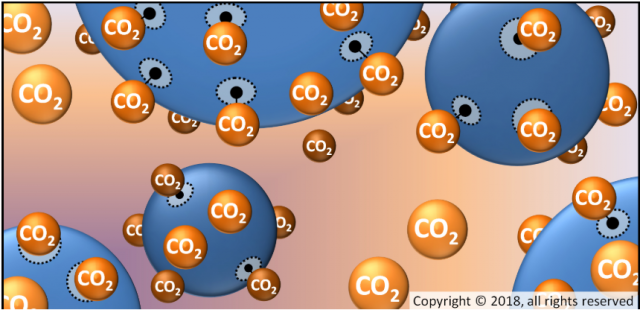
Vue d'artiste de l'interaction de composés carbonés (marron)
avec les interfaces huile (en bleu)/eau (en rose)
© 2018, all rights reserved. Denis Bendejacq, COMPASS,
CNRS / Rhodia / University of Pennsylvania, UMI 3254
Pourquoi la plupart des interfaces entre l'eau et une substance hydrophobe (huile, air, plastique, lipides, etc.) sont-elles chargées négativement ? Ce type d'interfaces étant omniprésent dans la nature (peau, cheveux, tissus, etc.), cette observation a souvent été faite, mais l'origine du phénomène anime un intense débat entre deux écoles de physico-chimistes depuis plus de quarante ans. Toutefois, un consensus pourrait avoir été trouvé grâce à la découverte impliquant des chercheurs de plusieurs laboratoires1 du CNRS pilotés par le laboratoire Ingénierie des matériaux polymères (CNRS/Université Jean Monnet/INSA Lyon/Université Claude Bernard). Selon eux, cette charge négative provient de l'action des ions bicarbonates présents naturellement dans l'eau ou issus de la transformation de CO2 atmosphérique. Leur structure chimique, des ions "encombrés" dont la charge est délocalisée entre ses différents atomes, leur confère une propension à se fixer sur des surfaces apolaires. La carbonatation de l'eau, souvent sous-exploitée, jouerait donc un rôle essentiel dans la physico-chimie des interfaces.
Cette découverte permet également d'expliquer un phénomène incompris jusqu'ici: la formation d'une émulsion (ici sous forme de petites gouttelettes d'huile) dans un mélange huile/eau soumis à des cycles répétés de gel et dégel. Lors de la congélation, le dioxyde de carbone présent dans l'air est piégé avant de se transformer en ions bicarbonates, stabilisant des gouttelettes d'huile en se collant à leur surface. Cette transformation de CO2 en bicarbonate pourrait intéresser d'autres domaines comme l'océanographie et notamment l'étude de la capture du CO2 par les océans.
Note:
(1) Ces travaux ont impliqué des scientifiques du laboratoire Ingénierie des matériaux polymères (CNRS/Université Jean Monnet/INSA Lyon/Université Claude Bernard), de l'Institut Charles Gerhardt Montpellier (CNRS/Université de Montpellier/ENSC Montpellier), du laboratoire Charles Coulomb (CNRS/Université de Montpellier) et de l'Institut Charles Sadron (CNRS).
Références publication:
X. Yan, A. Stocco, J. Bernard, F. Ganachaud
Freeze/Thaw-Induced Carbon Dioxide Trapping Promotes Emulsification of Oil in Water
Journal of Physical Chemical Letters – Octobre 2018
DOI: 10.1021/acs.jpclett.8b02919
X. Yan, M. Delgado, J. Aubry, O. Gribelin, A. Stocco, F. Boisson-Da Cruz, J. Bernard et F. Ganachaud
Central Role of Bicarbonate Anions in Charging Water/Hydrophobic Interfaces
Journal of Physical Chemistry Letters – Décembre 2017
DOI: 10.1021/acs.jpclett.7b02993
Contacts chercheur:
François Ganachaud, Complex Assemblies of Soft Matter (COMPASS UMI3254, CNRS/Rhodia/University of Pennsylvania)
Populaires